
Бесплатный фрагмент - Реабилитация при болезни Паркинсона
ОБ АВТОРЕ

Яковлев Алексей Александрович
Заведующий неврологическим отделением №2 клиники НИИ неврологии ФГБОУ ВО «ПСПбГМУ им. И. П. Павлова» МЗ РФ. Врач-невролог, врач-рефлексотерапевт, врач лечебной физкультуры и спортивной медицины, кандидат медицинских наук. Ассистент кафедры неврологии и мануальной медицины ФГБОУ ВО «ПСПбГМУ им. И. П. Павлова» МЗ РФ. Ассистент кафедры лечебной физкультуры и спортивной медицины ФГБОУ ВО «СЗГМУ им. И. И. Мечникова» МЗ РФ. Член Региональной общественной организации «Врачи Санкт-Петербурга», «Ассоциации неврологов Санкт-Петербурга», общероссийской общественной организации «Союз реабилитологов России». Автор более чем 75 научных публикаций по вопросам диагностики, лечения и реабилитации при различных неврологических заболеваниях. Высшее образование: ГБОУ ВПО «Санкт-Петербургская государственная медицинская академия им. И. И. Мечникова» МЗ РФ, врач, специальность «Лечебное дело» (2007), Санкт-Петербургский Инженерно-экономический университет, экономист-менеджер, специальность «Экономика и управление на предприятии здравоохранения», специализация — правовое регулирование хозяйственной деятельности (2011). В 2015 г. защитил кандидатскую диссертацию на тему: «Полинейропатия у пациентов с парапротеинемическими гемобластозами».
СПИСОК СОКРАЩЕНИЙ
АДР — агонисты дофаминовых (дофаминергических) рецепторов
АГТ — аутогенная тренировка
АТ — антитела
АТФ — аденозинтрифосфорная кислота
АХР — ацетилхолиновые рецепторы
ВОЗ — Всемирная Организация Здравоохранения
ВП — вызванный потенциал
ВЧБШ — внутренняя часть бледного шара
БДТЛ — болезнь диффузных телец Леви
БДУ — без дополнительных уточнений
БДН — болезнь двигательного нейрона
БОС — биологическая обратная связь
БП — болезнь Паркинсона
ГПО — грудопоясничный отдел позвоночника
ГЧС — гиперэхогенность черной субстанции
ДАД — диастолическое артериальное давление
ДТЛ — деменция с тельцами Леви
ДРД — диафрагмально-релаксационное дыхание
ЖКТ — желудочно-кишечный тракт
КБД — кортико-базальная дегенерация
КГР — кожно-гальванический рефлекс
КК — креатинкиназа
КОМТ — ингибиторы катехол-О-метилтрансферазы
КПМД — конечностно-поясная мышечная дистрофия
КР — коэффициент Ромберга
КТ — компьютерная томография
ЛКИГ — леводопа-карбидопа интестинальный гель
ЛЛПМД — лице-лопаточно-лицевая мышечная дистрофия
MAO — моноаминоксидаза
МВВ — миозит (миопатия) с внутриклеточными включениями
мДНК — митохондриальная дезоксирибонуклеиновая кислота
МКБ — международная классификация болезней
МКФ — международная классификация функционирования
МРТ — магнитно-резонансная томография
МРТР — 1-метил-4-фенил-1,2,3,6-тетрагидропиридина
MCA — множественная системная атрофия
МСЭ — медико-социальная экспертиза
НГЗ — назогастральный зонд
ОНМК — острое нарушение мозгового кровообращения
ОФЭКТ — однофотонная эмиссионная компьютерная томография
ПДС — позвоночно-двигательные сегменты
ПМР — пассивная мышечная релаксация
ПНМК — последствия нарушения мозгового кровообращения
ПНП — прогрессирующий надъядерный паралич
ППЯ — педункулопонтинное ядро
ПРФБС — поведенческое расстройство фазы быстрого сна
ПЭТ — позитронно-эмиссионная томография
рТМС — ритмическая транскраниальная магнитная стимуляция
РФ — Российская Федерация
САД — систолическое артериальное давление
СГСГМ — стимуляция глубоких структур головного мозга
СИОЗС — cелективные ингибиторы обратного захвата серотонина
СНМП — сверхнизкочастотные магнитные поля
СПБ — Синдром Пизанской башни
ССТ — Сниффин Стикс тест
СТЯ — субталамическое ядро
ТКС — транскраниальная сонография
ТПУ — тест Пенсильванского университета
ТСР — технические средства реабилитации
ЧМТ — черепно-мозговая травма
ЦНС — центральная нервная система
ЭМГ — электромиография
ОТ АВТОРА
Данное методическое пособие посвящено вопросам диагностики, медикаментозного лечения, а таже медицинской реабилитации при болезни Паркинсона. В пособие представлены как общие принципы нейрореабилитации при болезни Паркинсона, так и частные методики и технологии. Среди методов немедикаментозного лечения в отдельных главах уделено внимание применению методов лечебной физкультуры (в том числе кинезиотерапии, эрготерапии, фитбол-гимнастики, степ-гимнастики, танц-терапии, механотерапии и мн. др), физиотерапии, логопедии, психотерапии в процессе междисциплинарного взаимодействия при осуществлении медицинской помощи по профилю реабилитации пациентам с болезнью Паркинсона. Представленные в издании данные опираются на позиции доказательной медицины, официально утвержденные, в том числе нормативно-правовыми документами протоколы, алгоритмы, стандарты ведения пациентов, а также собственные наблюдения и разработки.
Методическое пособие предназначено для широкого круга специалистов, участвующих в построении междисциплинарного взаимодействия при оказании помощи по медицинской реабилитации пациентам с проявлениями болезни Паркинсона, в том числе организаторам здравоохранения, руководителям медицинских лечебно-профилактических учреждений, специалистам неврологам, реаниматологам, врачам лечебной физкультуры и спортивной медицины, врачам-физиотерапевтам, инструкторам-методистам лечебной физкультуры и инструкторам лечебной физкультуры со средним медицинским образованием, медицинским психологам, логопедам, среднему и младшему медицинскому персоналу, а также студентам клинических специальностей.
БОЛЕЗНЬ ПАРКИНСОНА: ПАТОГЕНЕЗ, КЛИНИКА И ДИАГНОСТИКА
Болезнь Паркинсона и паркинсонизм. Общие сведения, патогенез
Болезнь Паркинсона (БП) — хроническое прогрессирующее дегенеративное заболевание центральной нервной системы (ЦНС), клинически проявляющееся нарушением произвольных движений. Симптомы заболевания, похожего на БП, упоминаются еще с библейских времен. В Египетском папирусе XII века до нашей эры у одного из фараонов описаны симптомы заболевания, похожего на БП. В древнеиндийских текстах Аюрведы X века до нашей эры упоминается заболевание, проявляющееся тремором, нарушением движений, слюнотечением и другими симптомами, для лечения которых предлагаются некоторые виды бобовых (в частности — мукуна жгучая), которые содержат леводопу. Таким образом, вполне возможно, что пациенты с БП использовали преимущества леводопы еще на ранней стадии развития медицины. В древнеки-тайской литературе приводятся отдельные симптомы БП. Древнеримский врач Гален, ещё во II веке нашей эры описал тремор покоя. Леонардо да Винчи (1452—1519) упоминал в своих трудах о нарушениях движений и треморе. Более поздние упоминания, симптомов БП, были опубликованы в трудах ученых XVII — XVIII века Франциска Сильвия, Буасси де Соважа, Йоханнеса Батиста Сагара, Иеронима Гобия, Джона Хантера, Ференца Папая Париза, Калеба Хильера Парри.
Однако, первым кто подробно описал БП был английский врач Джеймс Паркинсон (англ. James Parkins—n, 11 апреля 1755 — 21 декабря 1824) в 1817 году опубликовавший свой труд «Эссе о дрожательном параличе» (рис. 1), в котором обобщил результаты наблюдений за шестью пациентами.

В настоящее время день рождения Джеймса Паркинсона стал Всемирным днем борьбы с данным заболеванием. В настоящий момент БП лидирует по распространенности среди нейродегенеративных заболеваний ЦНС. Джеймс Паркинсон (рис. 2) описывал данное заболевание, как «дрожательный паралич» со следующими характерными проявлениями: «непроизвольные дрожательные движения, ослабление мышечной силы, ограничение активности движений, туловище больного наклонено вперед, ходьба переходит в бег, при этом чувствительность и интеллект больного остаются сохранными». Спустя 70 лет после смерти Джеймса Паркинсона знаменитый французский невропатолог Жан Мартен Шарко назвал болезнь в честь его имени. В 1910 году Джорждем Баргером и Джеймсом Эвенсом впервые был синтезирован допамин, но многие годы он считался лишь предшественником норадреналина. И только в 1957 году шведский фармаколог Арвид Карлссон показал, что допамин является нейротрансмиттером головного мозга, а также разработал способ его измерения и нашел его самую высокую ре-гиональную концентрацию в базальных ганглиях. За что гораздо позже (2000 г.) он получил Нобелевскую премию по физиологии и медицине.

Принято различать понятие БП и паркинсонизма. Паркинсонизм — это синдром, ведущими клиническими проявлениями которого являются: гипокинезия (обязательный признак), мышечная ригидность, тремор покоя, постуральная неустойчивость. Паркинсонизм в свою очередь подразделяют на первичный, вторичный, а также паркинсонизм при мультисистемных дегенерациях ЦНС (таб. 1).
Согласно Международной статистической классификации болезней и проблем, связанных со здоровьем (МКБ — 10 пересмотра, 1995) выделяют:
G20 Болезнь Паркинсона
Гемипаркинсонизм
Дрожательный паралич
Паркинсонизм, или болезнь Паркинсона:
!БДУ
!идиопатический (ая)
!первичный (ая)
G21 Вторичный паркинсонизм
G21.0 Злокачественный нейролептический синдром
При необходимости идентифицировать лекарственное средство используют дополнительный код внешних причин (класс ХХ).
G21.1 Другие формы вторичного паркинсонизма, вызванного лекарственными средствами
При необходимости идентифицировать лекарственное средство используют дополнительный код внешних причин (класс ХХ).
G21.2 Вторичный паркинсонизм, вызванный другими внешними факторами
При необходимости идентифицировать внешний фактор используют дополнительный код внешних причин (класс ХХ).
G21.3 Постэнцефалитический паркинсонизм
G21.4 Сосудистый паркинсонизм
G21.8 Другие формы вторичного паркинсонизма
G21.9 Вторичный паркинсонизм неуточненный
G22 Паркинсонизм при болезнях, классифицированных в других рубриках
Сифилитический паркинсонизм (А52.1+)
Гепатолентикулярная дегенерация (E83.0)
Паркинсонизм при других нейродегенеративных заболеваниях (паркинсонизм-плюс)
Мультиситемная атрофия (G23.2)
Прогрессирующий надъядерный паралич (G23.1)
Деменция с тельцами Леви (G23.8)
Кортикобазальная дегенерация (G23.8)
Спиноцеребеллярные дегенерации (G11.2)
Болезнь Гентингтона (G10)
Палидарные дегенерации (G23.8)
Семейная кальцификация базальных ганглиев (G23.8)
В мире распространенность паркинсонизма на 100 тыс. населения составляет 120—180 случаев (в возрасте старше 60 лет — 1%), а заболеваемость 10—20 случаев на 100 тыс. населения. В Российской Федерации (РФ) распространенность паркинсонизма на 100 тыс. населения составляет 139,9 случаев, а в возрасте старше 40 лет этот показатель существенно возрастает до 268,2. Заболеваемость в РФ при этом составляет 16,9 случаев на 100 тыс. населения. Всего в РФ по разным данным, насчитывается от 117 до 338 тыс. больных БП. Предполагают, что с увеличением среднего возраста населения в ближайшие годы распространенность паркинсонизма в популяции будет увеличиваться. частота встречаемости основных форм паркинсонизма представлена в таб. 1.
С возрастом риск развития БП увеличивается, клинические проявления заболевания выявляются у 1% лиц старше 65 лет и у 2,6–4% лиц старше 85 лет. Дебют заболевания чаще всего происходит в возрасте 55–60 лет, средний возраст начала БП составляет 55 лет, при этом у 10% больных заболевание дебютирует в молодом возрасте до 40 лет (БП с ранним началом). Реже случаи развития болезни в более молодом возрасте дебют ювенильной формы проиcходит в возрасте до 20 лет. Продолжительность продромальной фазы БП варьирует, по разным оценкам, от 3 до 20 лет. Корреляция риска развития БП и возраста пациента связана, прежде всего, с тем, что с возрастом происходит ряд изменений, важных для функционирования нейронов чёрной субстанции. В частности, эти изменения затрагивают процессы метаболизма дофамина, а также включают снижение числа копий митохондриальной дезоксирибонуклеиновой кислоты (мДНК) дикого типа. Снижение количества копий мДНК дикого типа приводит к сокращению продукции аденозинтрифосфорной кислоты (АТФ) и снижению эффективной деградации белка, что тоже влияет на функционирование нейронов.
БП встречается чаще у мужчин, чем у женщин. При мета-анализе показано увеличение относительного риска развития БП у мужчин по сравнению с женщинами в 1,5 раза. Предполагается, что воздействие эндогенных и экзогенных эстрогенов вносит вклад в различия между полами. Известно, что эстрогены предотвращают истощение дофаминергических нейронов. Половые хромосомы способны независимо от половых стероидных гормонов влиять на развитие и поддержание дофаминовой системы. Как результат гормональных, хромосомных и других эффектов существует половой диморфизм базальных ганглиев и на молекулярных уровнях в дофаминергических нейронах, что может привести к различным патогенетическим механизмам у мужчин и у женщин. Таким образом, эстрогены и селективные модуляторы эстрогеновых рецепторов представляют собой нейропротекторы при БП.
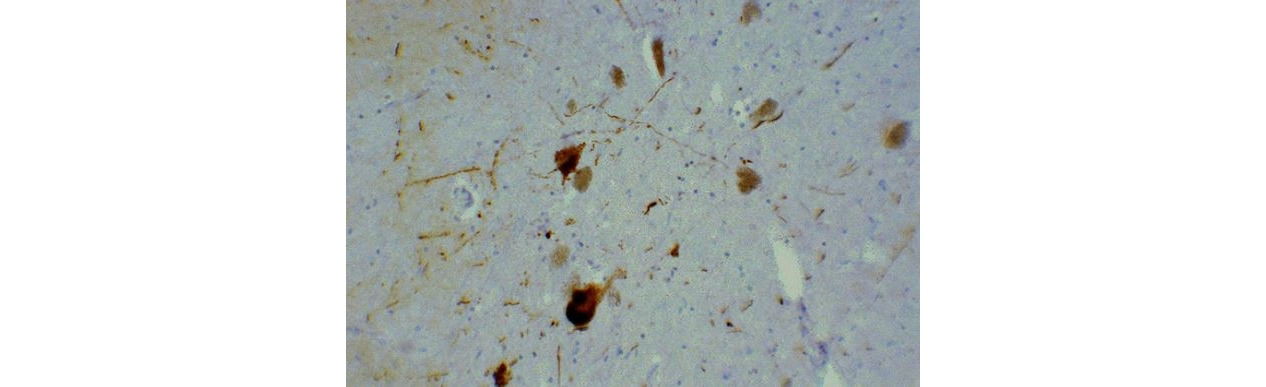
В основе патогенеза развития БП лежит повреждение дофаминергических нигростриарных нейронов и накопление альфа-синуклина (αSyn), содержащихся в тельцах Леви. Альфа-синуклеин является основным компонентом телец Леви. Нарушение процессинга αSyn является центральным звеном молекулярного патогенетического каскада, ведущего к накоплению в клетке нерастворимых белковых комплексов и прогрессирующей дегенерации соответствующей популяции нейронов при БП. Еще в 1919 году советский невропатолог Константин Николаевич Третьяков (рис. 3) связал развитие симптомов паркинсонизма с утратой пигментных нейронов черной субстанции ствола, а также с накоплением в этих клетках патологических включений (рис. 4). Нейрональные включения К. Н. Третьяков предложил называть тельцами Леви в честь немецкого морфолога Фридриха Леви, который ранее описал схожие изменения при паркинсонизме в других отделах ствола мозга.

Накопление αSyn рассматривается как основной момент в патогенезе БП, что отражено в полиморфизмах гена SNCA, ведущих к образованию аномального белка. Убедительным доказательством нейротоксичности αSyn стало получение на основе гиперэкспресcии гена SNCA человека трансгенных животных (дрозофила, мышь), демонстрирующих нейрональные αSyn-положительные включения и возрастную нейродегенерацию дофаминергических нейронов мозга.
Стоит заметить, что БП является преимущественно спорадическим заболеванием (90—95% случаев), семейный анамнез прослеживается всего лишь в 5—15% случаев по данным различных источников.
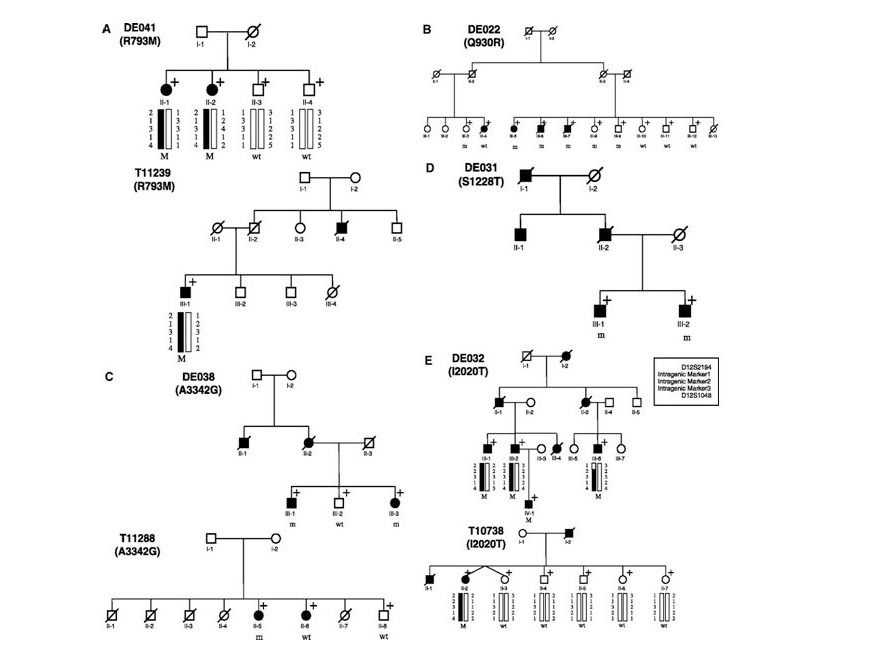
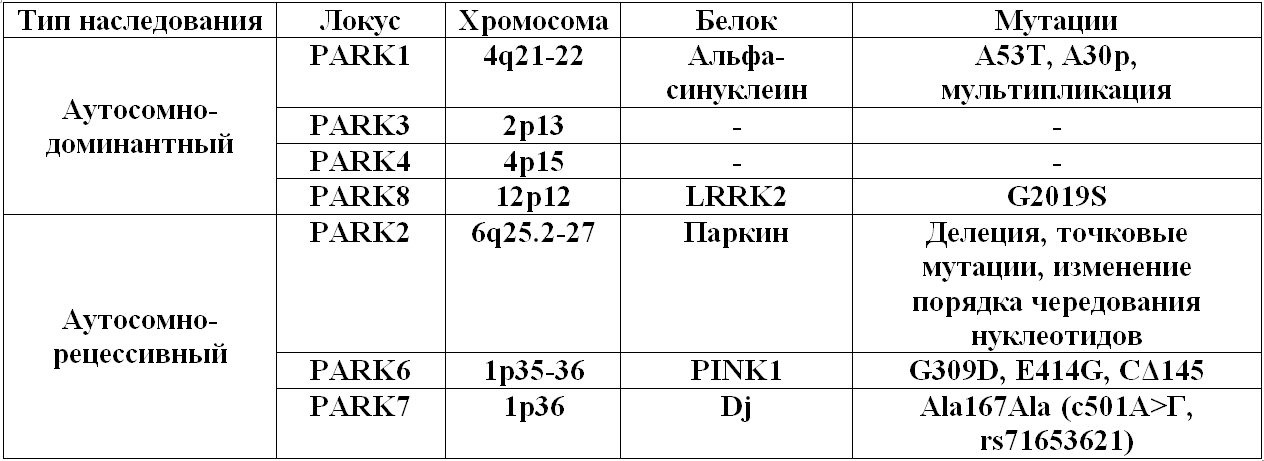
В настоящее время доказано, что наследственные варианты БП обусловлены мутациями генов SNCA, LRRK2, PRKN, DJ1, PINK1 и ATP13A2 и др. (рис. 5)
Мутация гена, расположенного на хромосоме 4q21—22, кодирующего белок αSyn, обуславливает развитие наследственной формы БП с аутосомно-доминантным типом наследования. Мультипликация генного локуса PARK1 увеличивает экспрессию αSyn и вызывает БП. Таким образом, можно утверждать, что повышение экспрессии αSyn токсично для нейронов.
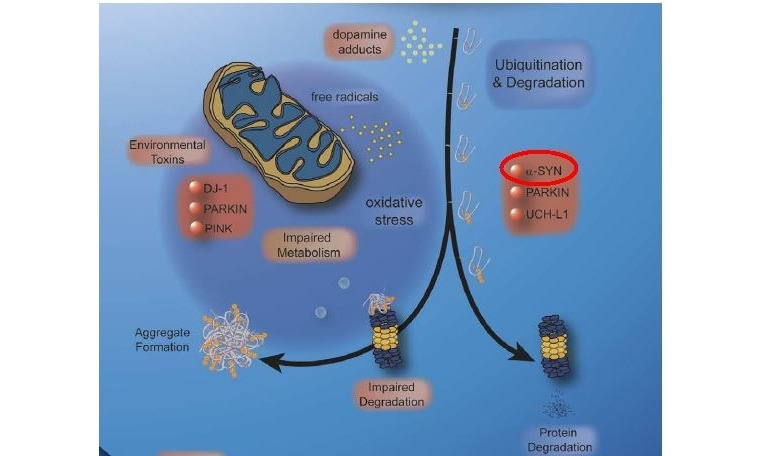
Также показано ингибирующее влияние αSyn на процесс мембранного слияния, который является важным биологическим механизмом поддержания базовой клеточной организации у эукариот. F. Kamp и соавт. (2010) на культуре клеток Caenorhabditis elegans (свободноживущая нематода) показали, что повышенная концентрация αSyn приводит к митохондриальной фрагментации, а также может смещать динамическое морфологическое равновесие митохондрий к уменьшенному слиянию. В свою очередь, митохондриальная фрагментация, вызванная экспрессией αSyn, возобновляется коэкспрессией PINK1, паркина или DJ-1, но не БП-ассоциированными мутациями гена PINK1 G309D, гена паркина Δ1—79 или гена DJ-1 C106A. Мутации в гене альфа-синуклеина (А53Т, А30Р) сопровождаются нарушением стабильности центральной части белковой молекулы, изменением её пространственной организации и формированием бета-складчатых слоев, способных аггрегировать с другими аналогичными молекулами с образованием мультимолекулярных фибрилл, что также нарушает процессы физиологического мембранного слияния.
Мутации генного локуса PARK2 связаны с развитием ювенильной БП с аутосомно-рецессивным типом наследования, болезни Альцгеймера, рака, сахарного диабета. В 1998 году был идентифицирован основной ген аутосомно-рецессивной ювенильной БП в хромосомной области 6q25.2—27, содержащий 12 экзонов, и кодирующий белок паркин, локализованный в комплексе Гольджи и цитозоле нейронов подкорковых ядер головного мозга. Наибольшая концентрация паркина обнаружена в пигментных клетках компактной зоны черной субстанции. Паркин обладает свойствами убиквитин-лигазы и играет ключевую роль в клеточной деградации аномальных белков. Мутации в гене паркина ведут к нарушению функций данного фермента в черной субстанции и стриатуме, что сопровождается накоплением аномальных белковых субстратов в клетке, индукцией апоптоза и гибелью нейронов.
В российском исследовании (Иллариошкин С. Н. и соавт., 2007 г.) с клинико-генетическим анализом 26 больных из 20 семей с возрастом дебюта БП до 30 лет были получены следующие данные: 41% семей имели мутацию гена паркина (PRKN). Всего было выявлено 9 мутаций: 6 из них были представлены делецией отдельных экзонов, 3-точковыми мутациями гена PRKN, ведущими к сдвигу рамки считывания (del202—203AG) или нарушению сплайсинга (IVS1+1G/А). T. Yoshida и соавт. (2010) на примере мутантных мышей (mnd2) показали, что введение таким мышам нормального белка паркина не влияет на течение нейродегенеративного процесса при БП.
Наиболее распространенной причиной моногенной формы БП с аутосомно-доминантным типом наследования является мутация гена LRRK2 (leucinerich repeat kinase 2), картированная на хромосоме 12q12, сцепленная с локусом PARK8 и кодирующая белок дардарин, функции которого изучены недостаточно (рис. 6). По некоторым данным, дардарин принимает участие в процессинге нейрональных белков, функционировании митохондрий и в межнейронных взаимодействиях. J. Vitte и соавт. (2010) исследовали экспрессию этого белка в мозге здоровых людей и людей, страдающих БП. Установлено, что эндогенный белок LRRK2 локализован в эндоплазматическом ретикулуме. До 24% белка обнаружено в клеточном ядре, в частности в 11% случаев — в тельцах Леви черной субстанции головного мозга. У пациентов, имеющих мутацию гена LRRK2 на хромосоме 12q12, концентрация исследуемого белка была увеличена до 50%. H. Mortiboys и соавт. (2010) провели исследование биоптатов кожи пяти пациентов, имеющих мутацию гена LRRK2 (G2019S), с целью изучения митохондриальных потенциалов, уровня внутриклеточной аденозин-трифосфатазы и продукции АТФ митохондриями нейронов. В результате исследования выявлена митохондриальная элонгация, снижение уровня продукции внутриклеточной АТФ, а также снижение мембранных потенциалов митохондрий.
Пациенты с БП имеющие мутацию гена LRRK2, как правило имеют классический вариант течения заболевания с типичным возрастом дебюта клинических проявлений и с хорошим ответом на препараты левадопы.
Мутации гена PTEN-индуцированной киназы 1 типа (PINK1) являются причиной семейной формы БП с аутосомно-рецессивным типом наследования. Белок PINK1, как полагают авторы, оказывает нейропротективный эффект на дофаминергические клетки, действуя как митохондриальная Ser/Thr протеин-киназа. На примере модели животных H.L. Wang и соавт. (2011) показали, что белок PINK1 необходим для поддержания нормальный митохондриального мембранного потенциала и митохондриальной морфологии допаминергических нейронов, а также этот белок оказывает нейропротективный эффект, ликвидируя формирование ROS. Мутации генных локусов PARK6 (G309D), E417G или CΔ145 гена PINK1 является дефектными в регулировании митохондриальных функций и уменьшении производства ROS дофаминергическими нейронами. Мутация в гене PINK1 приводит к изменению работы митохондрий нейронов, что, по мнению A. Berthier и соавт. (2011), связано с патогенезом БП.
Мутация генного локуса PARK7, кодирующего белок DJ1, приводит к развитию семейной формы БП с аутосомно-рецессивным типом наследования.
R.N. Alcalay и соавт. (2010) исследовали частоту встречаемости мутаций в причинных генах БП (PRKN, SNCA, PINK1, LRRK2, GBA). В исследование вошли 953 пациента, страдающего БП, с возрастом дебюта заболевания до 51 года. У 158 пациентов (16,6%) выявлены мутации, включая 64 PRKN (6,7%), 35 LRRK2 G2019S (3,6%), 64 GBA (6,7%) и 1 DJ1 (0,2%). Мутации были более частыми у пациентов с дебютом заболевания до 30 лет по сравнению с пациентами, имеющими более поздний дебют БП — между 31 и 50 годами (40,6%). Показана более высокая частота встречаемости мутации гена PRKN у испанского населения относительно других этнических групп (15,6% против 5,9%).
Исследование генома японского населения идентифицировало 2 новых локуса на хромосоме 1q32 (PARK16 и BST1), влияющих на предрасположенность к развитию БП. На примере корейского населения J.M. Kim и соавт. (2010) показали, что полиморфизмы генов DCC (rs17468382) и EPHB1 (rs2030737) могут быть связаны с увеличением риска развития БП, а полиморфизмы генов CHP (rs6492998) и RRAS2 (rs2970332) — с уменьшением риска развития БП.
Развитие БП сопровождается активацией фермента каспазы-3, стимулирующей процесс апоптоза нейронов.
T.H. Hamza и соавт. (2010) выполнили исследование всего генома 2000 пациентов, страдающих БП, и 1986 неврологически здоровых людей. Авторы подтвердили наличие ассоциации мутаций генов SNCA и MAPT, а также обнаружили новую ассоциацию с областью HLA. Ассоциация мутаций HLA была однородна во всех генетических и экологических группах риска. Пик ассоциации был в высоким в случает мутации rs3129882 — некодирующем варианте HLA-DRA. Предположительно, что мутация rs3129882 влияет на экспрессию генов HLA-DR и HLA-DQ. Головной мозг пациентов с БП чувствителен к воздействию антигенов DR и присутствию DR-позитивной реактивной микроглии, а нестероидные противовоспалительные средства (НПВС) уменьшают риск развития БП. Генетическая ассоциация с HLA подтверждает причастность иммунной системы в развитии БП и открывает новые горизонты для лечения этого заболевания.
J. Peng и соавт. (2010) показали существенное влияние экологических факторов на развитие, как спорадической формы БП, так и семейных (моногенных) форм заболевания (таб. 2).
Существует теория, что сварка может ускорять дебют БП, так как в процессе сварки образуются сложные металлические аэрозоли, ингаляция которых связана с неблагоприятным воздействием на нейроны. Так например, K. Sriram и соавт. (2010) на примере лабораторных крыс подтвердили дофаминергическую нейротоксичность марганца сварочного дыма.
J.M. Kim и соавт. (2010) показали роль мутации генов белков JMG2385R (rs34778348) и R1628P (rs33949390), богатых лейцином повторной киназы 2 (LRRK2, PARK8), в развитии спорадической формы БП среди населения Китая и Японии. В исследование были включены 923 пациента с БП и 422 здоровых лиц. Полиморфизм гена LRRK2 G2385R был обнаружен у 82 пациентов с БП (8.9% — гомозигота и 80% гетерозигота) и у 21 человека из группы контроля (5.0%, — все гетерозиготы). Частота встречаемости мутаций гена LRRK2 G2385R среди больных БП была значительно выше, чем в группе контроля. Гендерные различия между здоровыми носителями мутации G2385R и пациентами с БП, не имеющими исследуемую мутацию, а также разница среднего возраста начала заболевания, не выявлены. Мутация гена LRRK2 (R1628P аллельный вариант) встречалась значительно реже (0,78% у больных БП, 0,26% в группе контроля).
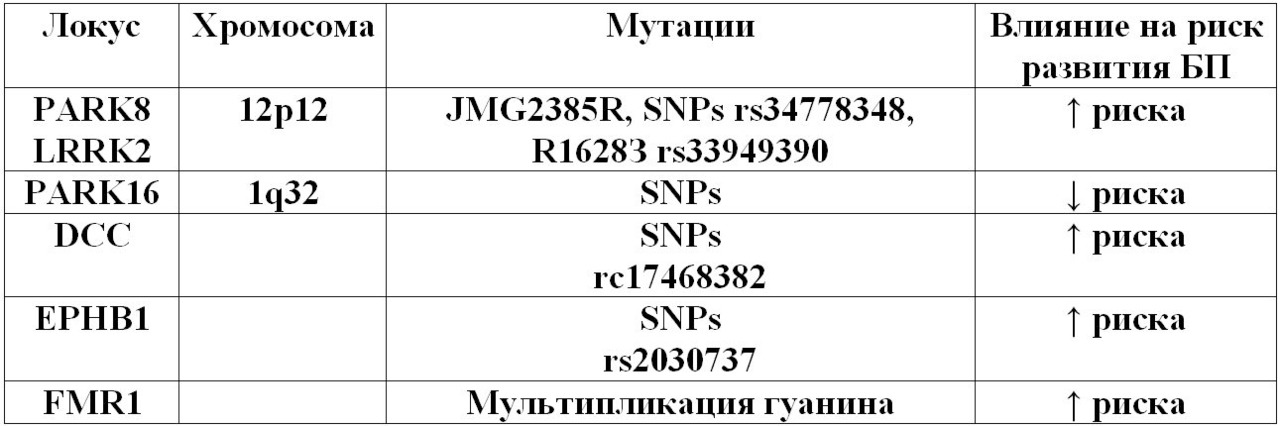
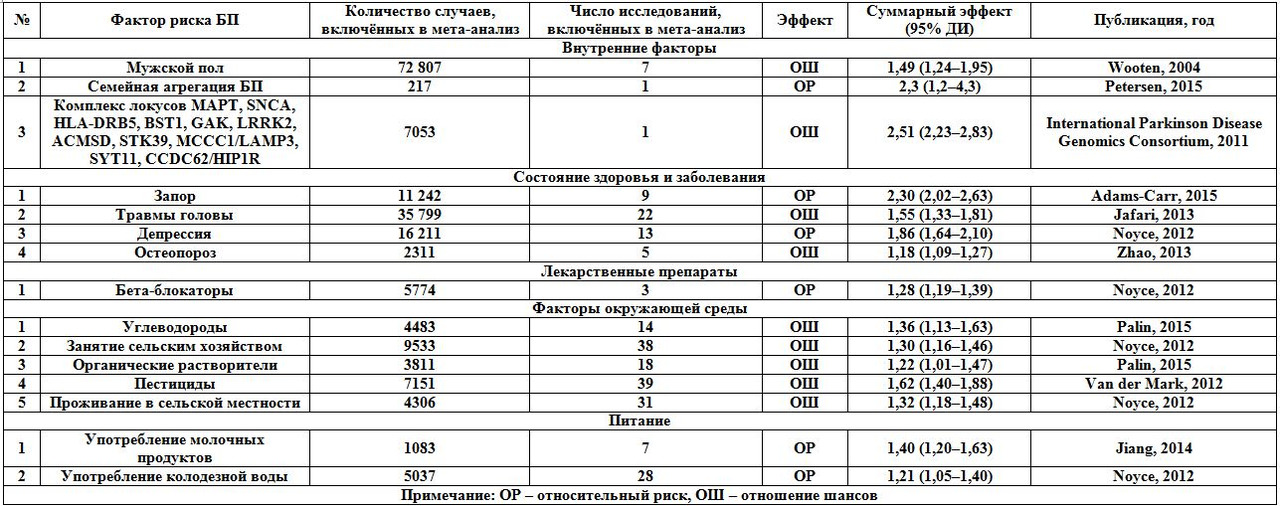
На сегодняшний день роль наследственного фактора в развитии БП несомненна, при всем изобилии генетических детерминант современные представления о БП базируются на том, что данное состояние является, прежде всего, мультифакториальным заболеванием (таб. 3), и наличие того или иного варианта мутации, может способствовать как повышению, так и снижению риска развития БП (таб. 4, 5). Кроме того, генетический фактор играет более важную роль в развитие БП с ранним началом.
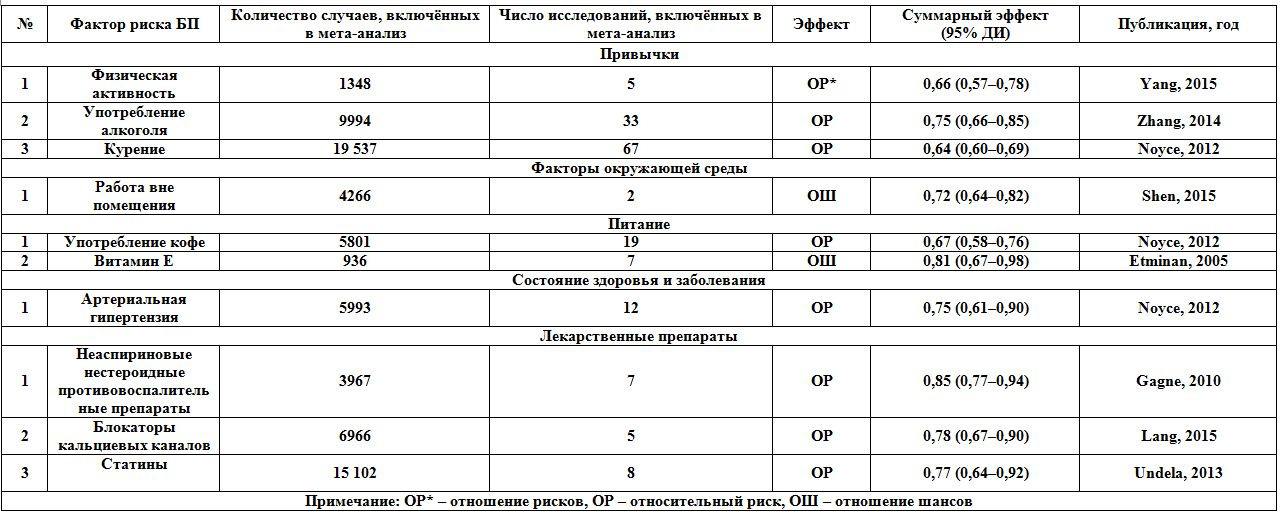
Внешние факторы, способные влиять на риск развития БП, можно распределить на 3 группы: 1) уменьшающие риск развития БП (физическая активность, употребление алкоголя, курение, работа вне помещения, употребление кофе, витамина E, гипертензия, нестероидные противовоспалительные препараты, блокаторы кальциевых каналов, статины); 2) увеличивающие риск БП (пожилой и старческий возраст, мужской пол, семейная агрегация БП, генетический компонент, углеводороды, занятие сельским хозяйством, органические растворители, пестициды, проживание в сельской местности, употребление молочных продуктов, колодезной воды, запоры, травмы головы, беспокойство, депрессия, остеопороз, лечение бета-блокаторами); 3) не оказывающие никакого влияния (магнитное поле сверхнизкой частоты, марганец, сварочные аэрозоли; употребление холестерина, углеводов, протеинов, жиров, чая, фолатов, витаминов A, B6, B12, C, D; сахарный диабет, рак, язвенная болезнь желудка, овариэктомия, подагра, общая анестезия, оральные контрацептивы, гормонозаместительная терапия в менопаузе).
Некоторые факторы, влияющие на риск возникновения БП, можно считать установленными, остальные — необходимо исследовать в будущем, так как влияние тех или иных внешних факторов на риск развития БП имеет различную степень доказательной базы.
Один из внешних факторов, который может быть потенциально связан с БП — это сверхнизкочастотные магнитные поля (СНМП). Поскольку многие работники подвергаются воздействию этих полей в дозах выше предельно допустимого уровня, такое излучение способно оказывать серьёзное влияние на общественное здоровье. Исследователи оценили действие СНМП на население и на профессионалов и получили противоречивые данные: одни результаты свидетельствовали о наличии связи СНМП с риском БП, другие — о её отсутствии. Мета-анализ не выявил увеличения риска БП из-за СНМП.
Несмотря на то, что имеются отдельные сообщения об ассоциации больших количеств марганца с развитием атипичного паркинсонизма, связь марганца с обычной формой БП более противоречива. Сварщики подвергаются воздействию марганца в составе сварочных аэрозолей, но остаётся неясным, достаточны ли его уровни для увеличения риска БП. Результаты мета-анализа данных когортных и кейс-контрольных эпидемиологических исследований показали, что сварочные аэрозоли и воздействие марганца не повышают риск БП.
В ряде работ выявлена положительная связь между воздействием углеводородов и развитием БП. Точный механизм потенциальной нейротоксичности углеводородов пока ещё неясен, хотя в экспериментах на животных установлен ряд повреждающих эффектов. У пациентов с БП и длительным воздействием органических растворителей в анамнезе при магнитно-резонансной спектроскопии были обнаружены повреждения нейронов полосатого тела, в то время как у лиц, не подвергавшихся действию этих веществ, подобных повреждений не найдено. Высказано предположение о существовании селективной чувствительности базальных ганглиев к повреждающему эффекту органических растворителей, которая подтверждалась статистически значимой зависимостью между уровнем их воздействия и степенью повреждения нейронов. По мнению некоторых авторов влияние углеводородов статистически значимо снижает связывание переносчика дофамина в наружной части чечевицеобразного ядра полосатого тела. Возможно, нейродегенерация возникает в результате сочетанного эффекта генетических и внешних факторов. Есть доказательства того, что генетические полиморфизмы ферментов, расщепляющих ксенобиотики, имеют значение для нейротоксичности углеводородов. Кроме того, предполагается, что в результате метаболизма углеводородов могут образовываться токсичные промежуточные соединения, которые индуцируют митохондриальную дисфункцию посредством усиления оксидативного стресса, что увеличивает риск БП.
В некоторых работах показан повышенный риск БП у лиц, проживающих в сельской местности и занимающихся сельским хозяйством. Эти данные могут быть объяснены влиянием пестицидов и других химических веществ. Литературные источники подтверждают гипотезу о том, что действие пестицидов или растворителей является фактором риска БП. Существует широкий спектр пестицидов, имеющих различный химический состав и механизм действия. Получены результаты, свидетельствующие о том, что гербициды и инсектициды, но не фунгициды, ассоциируются с развитием БП. Вместе с тем трудно разграничить эффекты гербицидов и инсектицидов, поскольку эти группы пестицидов, как правило используются одновременно. При этом работа вне помещения связана с уменьшением риска БП, что обусловлено, вероятно, большим количеством витамина D в организме людей, работающих на открытом воздухе.
В проспективном исследовании было установлено, что средний уровень дневной физической активности ассоциировался с пониженным риском БП. Её защитную роль при БП подтвердили эксперименты на животных, свидетельствовавшие о том, что принудительная физическая активность оберегает дофаминергические терминали и уменьшает двигательные аномалии. На крысиных моделях БП принудительные упражнения повышали содержание глиального нейротрофического фактора GDNF (который оказывал протективный эффект на дофаминергические нейроны, или снижал соотношение между переносчиком дофамина и белком-переносчиком везикулярного моноамина, что делало дофаминергические нейроны менее чувствительными к токсинам); а также восстанавливали дофаминергическую систему и увеличивали работоспособность дофаминергических нейронов в стриатуме, возможно посредством усиления высвобождения везикулярного дофамина или экспрессии D2-рецепторов. Предполагается, что у людей физические упражнения повышают уровень уратов в плазме, что, в свою очередь, ассоциируется с меньшим риском БП и более медленным прогрессированием заболевания. Кроме этого, отсутствие физической активности приводит к набору веса или ожирению, что вызывает уменьшение экспрессии D2-рецепторов в полосатом теле и тем самым увеличивает риск БП. Хотя потенциальные механизмы влияния различных типов физической активности полностью не ясны, исследования людей и животных демонстрируют её благоприятный биологический эффект в отношении риска развития БП. В проспективном исследовании 2014 года с участием 43000 человек продемонстрировано, что физическая активность в течение 6 часов в неделю уменьшает риск развития БП на 43% по сравнению с 2 часами физической активности.
В результате мета-анализа выявлено, что употребление алкоголя уменьшает риск БП и ассоциация связана с пивом в большей степени, чем с вином и крепкими напитками. Обратная связь риска БП и приёма алкоголя установлена у мужчин, но не у женщин. Употребление в день 50 г крепкого алкоголя на 5% снижает риск БП. Показано, что обратная связь приёма алкоголя с риском БП ослабевала, но оставалась значимой после корректировки по курению и по употреблению кофе.
Приём алкоголя может воздействовать на риск возникновения БП непосредственно или путём влияния на содержание мочевой кислоты в сыворотке крови, поскольку уровень этого показателя обратно связан с развитием БП и способен отсрочить её прогрессирование.
Результаты мета-анализа свидетельствуют, что курение является протективным фактором в отношении развития БП. Кроме того, установлена статистически значимая обратная зависимость риска БП от индекса курения. Табак и табачный дым содержат более 9000 химических компонентов, среди которых именно никотин стимулирует дофаминергические нейроны, тем самым обладая нейропротективным действием. Никотин оказывает эффект на периферическую и центральную нервную систему, стимулируя никотиновые ацетилхолиновые рецепторы. D.P. Hong и соавт. исследовали влияние никотина и 4 других компонентов сигаретного дыма (анабазин, котинин, гидрохинон и норникотин) на фибрилляцию αSyn белка, который агрегируется в тельцах Леви при БП наряду с другими белками.
Никотин и гидрохинон ингибируют образование αSyn фибрилл (при этом никотин более эффективен). Эти составляющие стабилизируют растворимые олигомерные формы αSyn.
Некоторые специалисты предполагают, что фермент моноаминоксидаза B (MAO-B), который играет роль в биоактивации индуцирующего паркинсонизм нейротоксина 1-метил-4-фенил-1,2,3,6-тетрагидропиридина, ингибируется в мозгу курильщиков.
Ожирение — хорошо известный фактор риска различных метаболических и сосудистых расстройств. В результате мета-анализа 10 проспективных исследований не обнаружено ассоциации между индексом массы тела и риском БП. Мета-анализ выявил, что наличие в анамнезе травм головы, сопровождавшихся потерей сознания, статистически значимо связано с повышенным риском БП. Предложено несколько возможных механизмов этой взаимосвязи. Наиболее правдоподобным представляется нейровоспаление, вызванное травмой, которое вносит вклад в патогенез БП. Травма головы может привести к разрушению гематоэнцефалического барьера и вызвать лейкоцитарную инфильтрацию и активацию микроглии, а также нарушение функции митохондрий и усиление интоксикации глутаматом, что способствует развитию нейродегенеративных заболеваний, в том числе БП. Тяжёлые травмы головы следует рассматривать в качестве одного из основных факторов возникновения БП.
Связанный с БП запор может быть обусловлен образованием телец Леви в нервной системе кишечника или дорсальных двигательных ядрах блуждающего нерва, которые поражаются в наиболее ранние сроки развития БП. При исследовании в группе пожилых мужчин редкие движения кишечника по данным самооценки были связаны с высоким риском БП и уменьшением плотности нейронов чёрной субстанции. Является ли запор самостоятельным фактором риска БП или ранним симптомом в продромальной фазе заболевания, остаётся предметом споров. Наличие запора, наряду с другими немоторными симптомами, способно служить признаком для идентификации индивидуумов с повышенным риском БП.
Результаты когортных исследований сахарного диабета, как фактора риска БП противоречивы. В некоторых работах выявлены статистически значимая положительная ассоциация риска БП с беспокойством и депрессией и значимая отрицательная ассоциация с артериальной гипертензией. Расстройства настроения связаны с вовлечением ствола мозга, что (наряду с вовлечением обонятельного центра) случается в ранней фазе БП. Наиболее выраженными факторами риска развития БП были семейный анамнез БП и тремор. Не установлено связи риска БП с раком.
Наличие хирургической менопаузы существенно изменяло риск БП, но необходима дальнейшая работа в этом направлении, так как исследования случай-контроль продемонстрировали статистически значимое снижение риска, а когортные — его статистически значимое увеличение.
Предполагалось, что Helicobacter pylori — возможный фактор риска БП, однако исследования этой связи отсутствуют. Вместе с тем не выявлено ассоциации предшествующей язвенной болезни желудка (которая может быть суррогатным маркёром данной инфекции) с последующим развитием БП. Мочевая кислота является антиоксидантом, а гиперурикемия коррелирует с пониженным риском БП; но при мета-анализе не обнаружено обратной связи между подагрой и риском БП. Результаты некоторых исследований свидетельствуют, что риск развития остеопороза выше у пациентов с БП по сравнению со здоровыми лицами контрольной группы, а также у мужчин с БП по сравнению с женщинами, страдающими этим заболеванием.
Мета-анализ указывает на то, что у пациентов с БП плотность кости в области таза, поясничных позвонков и шейки бедра ниже, чем у здоровых лиц референтной группы.
Приём бета-блокаторов увеличивал риск развития БП. Это, однако, можно объяснить их применением для лечения изолированного тремора. Блокаторы кальциевых каналов ассоциированы с уменьшением риска.
При исследовании статинов также был продемонстрирован тренд снижения риска БП, который может быть обусловлен их протективным эффектом в отношении оксидативного стресса. Приём нестероидных противовоспалительных препаратов уменьшал риск БП примерно на 17%, что свидетельствует о существенной роли воспаления в патогенезе этого заболевания. Не было обнаружено никакой связи между приёмом оральных контрацептивов или гормонозаместительной терапией в менопаузе (постменопаузе) и развитием БП, хотя эти вопросы требуют дальнейшего изучения, поскольку исследования случай-контроль показали статистически значимое снижение риска, тогда как когортные — его статистически значимое повышение.
Патоморфологические стадии развития болезни Паркинсона
В настоящее время существует концепция постадийного клинического развития БП, в основу которой легла гипотеза H. Braak, сформулированная в 2003 году. Согласно этой гипотезе, основанной на патоморфологическом изучении — синуклеин-содержащих изменений, у больных с различной тяжестью БП и лиц, не имеющих при жизни признаков паркинсонизма, болезнь прогрессирует на протяжении 6 стадий. Нейродегенеративный процесс при БП может начинаться с появления телец Леви в периферических вегетативных мезентериальных сплетениях, распространяясь центропетально, затем восходя от каудальных отделов головного мозга к коре (Таб. 6).

На I стадии патологический процесс затрагивает дорсальное моторное ядро Х нерва, обонятельную луковицу с прилегающей частью переднего обонятельного ядра, что обуславливает появление в клинической симптоматики самых ранних признаков заболевания — гипосмию и дисфункцию желудочно-кишечного тракта (констипацию).
На II стадии при распространении дегенеративного процесса на ядра шва, части ретикулярной фармации и голубоватое пятно появляются сенсорные изменения, в частности, болевые проявления, эмоциональные расстройства.
На III стадии процессом затрагивается черная субстанция, но без гибели нейронов, а также миндалина, педункулопонтинные ядра, оральное ядро шва, холинэргические магноцеллюллярные ядра базальных отделов переднего мозга, туберомамиллярные ядра гипоталамуса, что проявляется нарушением REM-фазы сна (rapid eye movement — быстрые движения глаз, т. е. фаза быстрого сна), аффективными расстройствами, депрессией.
На IV стадии происходит снижение количества нейронов в компактной части черной субстанции, приводящее к двигательным нарушениям. Кроме того, на этой стадии в патологический процесс вовлекается переходная зона между древней и новой корой, через которую следуют проекции первичных зон коры к префронтальной коре, что влечет за собой когнитивный дефицит в виде ослабления памяти и утраты личностной инициативы, проявления вторичной лобной дисфункции.
На V стадии происходит нарастание когнитивных нарушений с одновременным появлением психотических расстройств вследствие вовлечения в процесс структур неокортекса, прежде всего, ассоциативных зон в префронтальной, височной и теменной коре.
На VI стадии происходит усугубление изменений в ранее пораженных структурах с вовлечением первичных сенсорных и моторных зон коры. О «периферическом» генезе БП стали говорить, когда было показано, что в латентном периоде БП нейродегенеративные «паркинсонические» изменения (агрегаты α-синуклеина, тельца Леви) выявляются в периферических вегетативных нейронах: в клетках нервных сплетений кишечника, пре- и паравертебральных ганглиях, в дистальных симпатических терминалях и ганглиях симпатического ствола, нейронах надпочечников, слюнных желез, кожи и т. д.. Одной из теорий предполагается, что вовлечение парасимпатических интрамуральных нейронов кишечника и клеток обонятельных ядер может быть наиболее ранними патологическими событиями при БП, которые указывают на возможность вдыхания и/или алиментарного поглощения триггерного патогена. Дальнейшее распространение патологического процесса может происходить по волокнам обонятельного и блуждающего нервов (с поражением соответствующих нейронов каудального ствола), а также по механизмам ретроградного аксонального транспорта (в периферической вегетативной нервной системе — см. рис. 7).
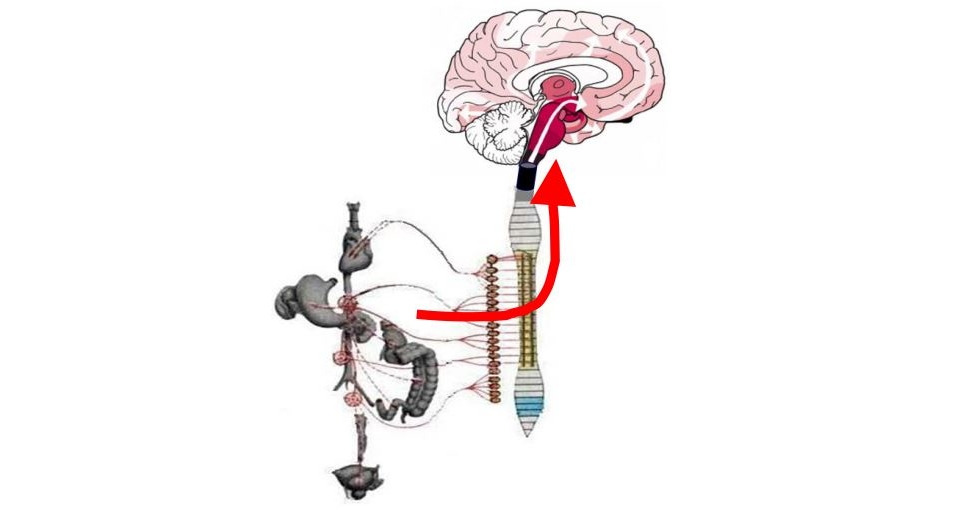
Клинические стадии развития болезни Паркинсона
В классификации БП выделяют клиническую форму, стадию и темп прогрессирования.
В зависимости от доминирования в клинике того или иного симптома выделяют три клинических формы: акинетико-ригидно-дрожательную (60—70%), акинетико-ригидную (15—20%) и дрожательную (5—10%).
В отношении клинической стадии заболевания общепризнанной является следующая классификация стадий (степеней тяжести) БП:
Стадия 0. Двигательные проявления отсутствуют;
Стадия 1. Односторонние проявления заболевания;
Стадия 2. Двусторонние проявления заболевания без постуральной неустойчивости;
Стадия 3. Умеренно выраженная постуральная неустойчивость, возможно самостоятельное передвижение;
Стадия 4. Значительная утрата двигательной активности, но пациент в состоянии передвигаться;
Стадия 5. При отсутствии посторонней помощи пациент прикован к постели или инвалидному креслу.
Выделяют также модифицированную шкалу Хен и Яр (Hoehn, Yahr, 1967), которая впервые была опубликована в журнале «Neurology» Маргарет Хён и Мелвином Яром и официально утверждена в 1967 году.
Модифицированная шкала Хен и Яр
Стадия 0.0 — нет признаков паркинсонизма (данная стадия характеризуется отсутствием клинических проявлений заболевания, однако в центральной нервной системе уже начинаются структурные изменения. Болезнь на этой стадии диагностируется очень редко, как правило, случайно);
Стадия 1.0 — только односторонние проявления (у больных наблюдают односторонний тремор кисти руки, тремор имеет слабо выраженный характер. По мере прогрессии появляются изменения осанки, мимики лица, походки, может появляться боль в плечевом суставе на стороне поражения. Также может появиться ощущение «песка в глазах», вследствие сокращения количества мигательных движений век. У пациентов увеличиваются затраты времени на бритье, расчесывание и другие ежедневные манипуляции);
Стадия 1.5 — односторонние проявления с вовлечением аксиальной мускулатуры (происходят локомоторные изменения, сокращение амплитуды движений, появляется выраженная ригидность мышц лица и шейного отдела);
Стадия 2.0 — двухсторонние проявления без признаков нарушения равновесия (расстройства носят двусторонний характер и проявляются дрожанием кистей рук, недостаточной амплитудой и скованностью. Возникает непроизвольное покачивание головы, а ригидность лицевой мускулатуры приводит к гипомимии («маскообразное» лицо);
Стадия 2.5 — мягкие двухсторонние проявления. Сохранена способность преодолевать вызванную ретропульсию;
Стадия 3.0 — умеренные или средней тяжести двухсторонние проявления. Небольшая постуральная неустойчивость. Но больной не нуждается в посторонней помощи (становится более выраженной ретропульсия. У пациентов прогрессирует скованность движений, в результате потери равновесия возможны падения. При ходьбе больной прижимает руки к телу, сокращается длина и высота шага — признак «шаркающей» походки. Несмотря на симптоматику, человек продолжает себя обслуживать, сохраняется частичная способность работать);
Стадия 4.0 — тяжёлая обездвиженность; однако ещё может ходить или стоять без поддержки (развивается значительная гипокинезия, выраженный тремор головы и конечностей. Иногда тремор уменьшается. Больной не в состоянии выполнять физическую работу, уход за собой вызывает существенные затруднения. Движения выполняются с трудом, походка становится очень медленной. На этом этапе пациенту необходимы дополнительные средства, чтобы поддерживать равновесие — трость, костыли, ходунки);
Стадия 5.0 — без посторонней помощи прикован к креслу или кровати (данная стадия заболевания характеризуется потерей возможности самостоятельно передвигаться. Больной перемещается при помощи инвалидного кресла, либо он все время лежит в кровати. С этого момента человек нуждается в постоянном уходе со стороны близких или медицинского персонала. Появляются выраженные нарушения глотательной функции, что ведет к потере веса).
Кроме того, при БП принято выделять три вида темпа прогрессии заболевания: быстрый, умеренный и медленный. При быстром темпе смена стадий заболевания (первая — вторая/вторая — третья) происходит в течение 2 и менее лет. При умеренном темпе смена стадий происходит более чем за 2 года, но не более чем за 5 лет. При медленном темпе смена стадий происходит более чем через 5 лет.
Клиническая картина болезни Паркинсона
Клинические проявления БП принято разделять на моторные и немоторные. Среди моторных симптомов заболевания следует выделить: брадикинезию, ригидность, тремор покоя, постуральную неустойчивость. К немоторным проявлениям БП относят: нарушения обоняния, вегетативные проявления (дисфункция желудочно-кишечного тракта, мочеиспускания, половую дисфункцию, нарушение потоотделения, постуральную гипотензию, себорею), аффективные нарушения, нарушения сна, психотические нарушения, когнитивные нарушения.
Гипо- или брадикинезия при БП.
Брадикинезия при БП проявляется замедленностью движений, уменьшением амплитуды движений, нарушением инициации движений, истощаемостью (декремент) движений, асимметрией (в начале болезни может быть только в одной конечности или ее сегменте), гипомимией, редким миганием, укорочением длины шага, замедленностью ходьбы, затруднением при вставании, поворотах и т. д., микрографией, нарушением мелких движений (чистка зубов, печатание, набор номера телефона), брадилалией, гипофонией, диспросодией (монотонность), иногда тахифемией (ускоренная речь с элементами многословия).
Для стереотипа походки при БП характерны следующие признаки: приволакивание одной ноги при ходьбе, ахейрокинез (симптом ролекса), микробазия (укорочение шага), шарканье, ускорение ходьбы — за счет частоты шагов, пропульсии, пародоксальные кинезии, застывания (freezing) — чаще при изменении программы ходьбы, топтание на месте.
Мышечная ригидность при БП.
Мышечная ригидность при БП может иметь следующие характеристики: пластический тип, тип «зубчатого колеса», развивается во всех мышечных группах (агонисты и антагонисты), в аксиальной мускулатуре, нарастает по мере проверки, асимметрична, в начале болезни чаще представлена в дистальных отделах рук, в шее, усиливается при движениях в других конечностях.
Тремор при БП.
Классическим вариантом тремора при БП является тремор покоя, развивающийся чаще в дистальном отделе рук, усиливающийся при движениях другими конечностями и при ходьбе, характерен паттерн по типу «скатывание пилюль» или «счет монет», тремор носит асимметричный характер, у части больных постуральный тремор или кинетический тремор, тремор возобновляется при удержании позы
Выделяют следующие виды тремора при БП:
1. Тремор покоя 3-6-Гц и постурально-кинетический той же частоты;
2. Тремор покоя 3-6-Гц и постурально-кинетический высокой частоты (до 9 Гц);
3. Изолированный постурально-кинетический высокой частоты (до 9 Гц);
4. Изолированный тремор покоя.
Постуральные нарушения при БП.
Постуральная неустойчивость — это неспособность удерживать равновесие при изменении положения тела или ходьбе. У пациентов с БП смещение центра тяжести при изменении позы не вызывает компенсаторных движений (ходьба, вставание, повороты на одном месте, ходьба назад, наклон вперед). Для определения постуральной неустойчивости рекомендуется проводить толчковую пробу или пробу Тевенара. Данная проба предложена французским неврологом A. Thevenard (1898—1959). Проводится проба следующим образом: стоящего больного выводят из состояния равновесия, подталкивая вперёд или назад, врач обычно становится за спиной больного и рывком за плечи тянет его на себя. Больные с постуральной неустойчивостью при этом падают или, пытаясь всё же удержать равновесие, делают несколько мелких шажков вперёд (пропульсия) или назад (ретропульсия). Нормой является — не более 2-х шагов для удержания равновесия. К постуральным нарушениям при БП также будет относится: изменения позы, преобладание тонуса в сгибательной мускулатуре — поза «просителя» (сгибательная поза), камптокармия (camptocormia; греч. campto — гнуть, сгибать и kormos — туловище) — выраженный наклон туловища вперед, антероколлис, наклон туловища вбок, сколиоз (симптом Пизанской башни).
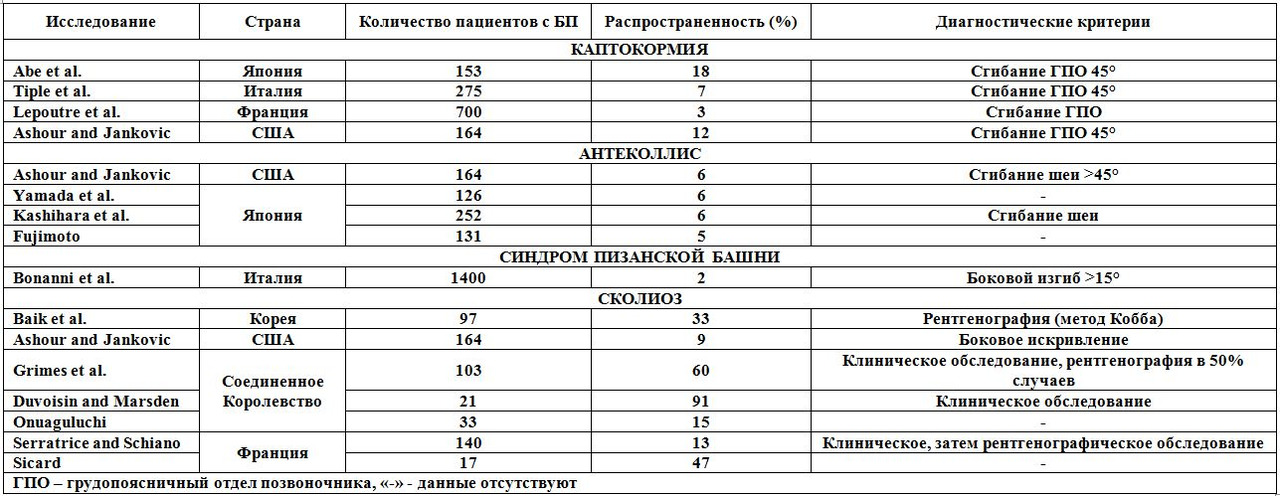
Для описания согнутого позвоночника у пациента с БП термин «камптокормия» впервые использовали в 1999 г.. В ряде исследований описаны показатели распространенности камптокормии при БП в пределах от 3 до 17,6% (Таб. 7). Такой широкий диапазон, вероятно, обусловлен различными пороговыми значениями, используемыми для диагностики камптокормии, а также вследствие отсутствия точного клинического определения и различий изучаемых популяций. Результаты эпидемиологических исследований указывают на то, что распространенность камптокормии может быть выше у азиатов, что может отражать генетические различия в строении скелета между различными этническими группами. Большинство исследователей сообщают о наличии положительной связи между камптокормией и тяжестью заболевания. У пациентов с камптокормией наблюдают тенденцию к более тяжелому течению паркинсонизма, чем у лиц без этой деформации. Камптокормию также чаще выявляют у пациентов более старшего возраста. В среднем камптокормия формируется спустя 7—8 лет после начала развития паркинсонизма.
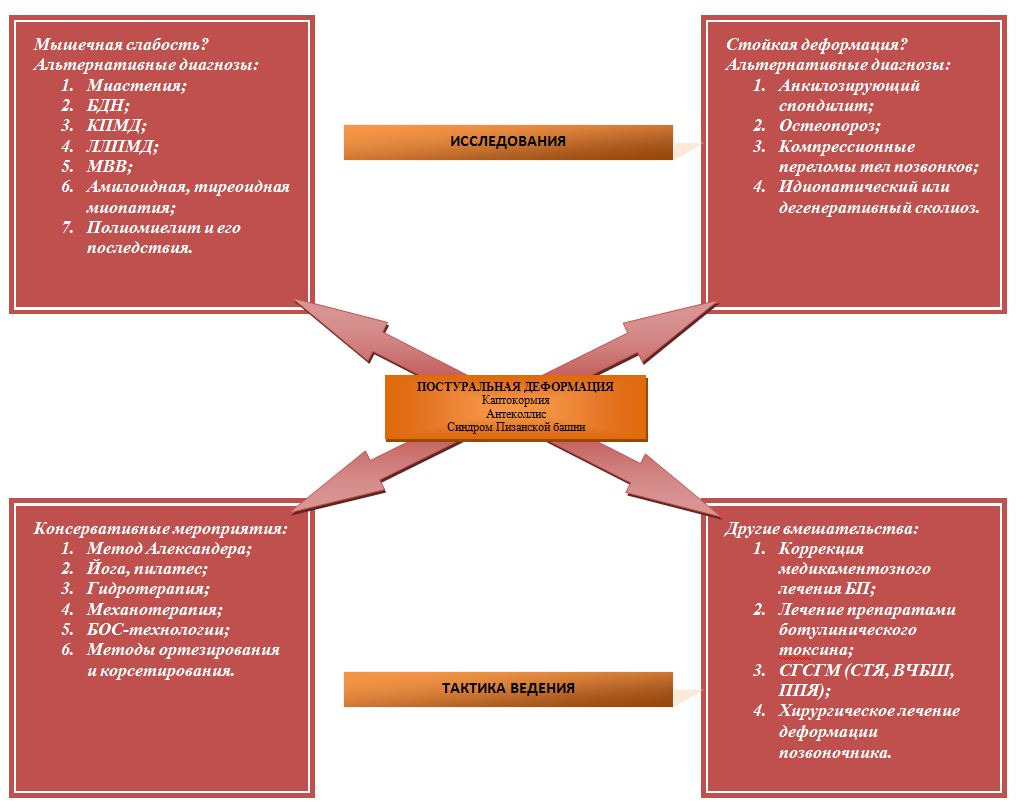
Диагностика камптокормии при паркинсонизме основана только на результатах клинического обследования, поскольку исследование этиологических причин деформации затруднено вследствие недостатка знаний в этой области. Тем не менее некоторые специфические признаки могут указывать на альтернативный диагноз. Например, слабость при выпрямлении туловища свидетельствует о наличии сопутствующей миопатии или поражении клеток переднего рога, что должно инициировать дальнейшее обследование в этом направлении. Постоянная деформация, которая сохраняется даже в положении лежа на спине, указывает на наличие костно-суставных изменений, которые могут быть как ее причиной (например, перелом позвоночника, анкилозирующий спондилит) или развиваться вторично по отношению к деформации (например, приобретенная дегенеративная спондилоартропатия). Список диагнозов, вероятность которых следует рассматривать, а также дополнительные исследования, к подбору которых необходимо подходить индивидуально, представлен на рис. 8.
Под антеколлисом при паркинсонизме подразумевают сгибание вперед головы и шеи. Если антеколлис легко выражен, его можно рассматривать, как элемент сутулой позы при БП, но у некоторых пациентов отмечают так называемый непропорциональный антеколлис: шея свисает вперед больше, чем ожидается, по сравнению с согнутым положением туловища и конечностей. Термин «синдром свисающей головы» (dropped head syndrome) иногда используют для описания выраженного изгиба шеи, но гораздо более часто он относится к таким нейромышечным заболеваниям, как миастения (myasthenia gravis), полимиозит и болезнь двигательного нейрона (БДН), при которых данное состояние связано со слабостью мышц-разгибателей шеи (что непосредственно приводит к свисанию головы вперед).
Антеколлис лишь недавно стали рассматривать как проявление паркинсонизма. Его считают сравнительно распространенным проявлением множественной системной атрофии (MCA), при которой антеколлис относительно постоянный, в отличие от идиопатической спастической кривошеи. В ретроспективном исследовании Ashour и Jankovic указывают на высокую распространенность этой деформации (42,1%) у пациентов с MCA, тогда как средний показатель распространенности при БП гораздо меньше — 5,8%. При изучении серии клинических случаев (15 больных с болезнью Паркинсона) антеколлис чаще выявляли у женщин, а также у пациентов, у которых выраженными признаками паркинсонизма были ригидность и акинезия. Как и при других постуральных деформациях, этническое происхождение исследуемой популяции влияет на распространенность — больше всего случаев антеколлиса зарегистрировано в Японии.
Антеколлис может развиваться подостро в течение недель или месяцев. Он может возникать до появления других двигательных проявлений БП, но чаще развивается через несколько лет после начала заболевания. Пациенты могут жаловаться на боль по задней поверхности шеи или на проблемы, возникающие в связи со сгибанием шеи (затруднение глотания, избыточное слюнотечение или ограничение поля зрения). Антеколлис при БП часто ассоциируется со значительным повышением тонуса аксиальных мышц, хотя у некоторых пациентов еще остается возможность пассивного разгибания до нормального положения. У других пациентов антеколлис может перейти в постоянную деформацию, даже спустя короткое время после начала развития.
Дополнительные диагностические исследования при антеколлисе необходимо назначать на основании результатов физикального обследования. По мере увеличения давности существования деформации антеколлис часто ассоциируется с ограничением диапазона движений, но в тех случаях, когда существенное ограничение движений шеи возникает подостро или интенсивность боли не соответствует таковой при антеколлисе, необходимо проведение визуализации для исключения патологии шейного отдела позвоночника. При выявлении антеколлиса наиболее распространенной альтернативой БП является МСА, при которой антеколлис — частое явление. В недавних сообщениях также обращают внимание на возможное влияние медикаментозного лечения на положение шеи. Антеколлис может представлять собой явление, развивающееся в отсутствие приема препаратов, или возникающее при повышении дозы дофаминергических лекарственных средств, так же, как дискинезии, поэтому необходимо исследовать изменения выраженности антеколлиса и взаимосвязь этих изменений с периодами приема и отмены лекарственных средств. Существует несколько сообщений о случаях, когда развитие антеколлиса могло быть индуцировано приемом агонистов дофамина (7 пациентов получали прамипексол, 5 — каберголин, 2 — перголид; в 2 случаях лекарственное средство не было идентифицировано) или применением амантадина. Поэтому при наличии тесной взаимосвязи времени начала приема указанных препаратов и развития антеколлиса необходимо прервать прием этих лекарственных средств в качестве диагностической пробы, хотя следует учитывать, что антеколлис не обязательно обратим, особенно в тех случаях, когда до отмены препарата лечение проводили в течение длительного времени.
Наличие у пациента мышечной слабости при исследовании остаточного разгибания шеи должно побуждать к проведению обследования для выявления нейромышечной патологии. Если пациенты сообщают о двоении в глазах или о симптомах, указывающих на повышенную утомляемость, необходимо рассмотреть вероятность наличия миастении. Опубликовано небольшое количество сообщений, в которых описано коморбидное течение БП и миастении у пациентов с антеколлисом. Мышечная слабость при разгибании шеи также может быть проявлением болезни двигательного нейрона. У пациентов с БП и антеколлисом, но без слабости, отклонения от нормы могут быть выявлены при проведении электромиографии (ЭМГ) и биопсии мышц, но данные исследования часто неспецифичны и не имеют диагностической ценности для определения того, являются они причиной развития антеколлиса или его следствием.
Синдром Пизанской башни (СПБ) — это выраженный боковой изгиб туловища, который обычно не является фиксированным (например, исчезает в положении лежа). Впервые СПБ был описан, как дистония туловища, или плеврототонус (плеврототонус (pleurothotonus) — разновидность тетанических судорог, при которых происходит отклонение туловища вбок, в отличие от отклонения вперед (эмпростотонус), назад (опистотонус) или застывания тела в выпрямленном положении (ортотонус)), встречающаяся в виде побочного эффекта антипсихотического лечения. Позднее СПБ был описан при БП. Помимо этого он был описан у пациентов с болезнью Альцгеймера, которые получали ингибиторы холинэстеразы. СПБ встречается также как идиопатический феномен и может предшествовать развитию сколиоза при БП.
Диагностических критериев СПБ не существует, хотя Bonanni et аl. предложили следующие критерии определения боковой аксиальной дистонии: боковое сгибание туловища более 15°, которое нарастает во время ходьбы и нивелируется в положении лежа на спине при отсутствии каких-либо механических ограничений для движений туловища (например, дегенеративные заболевания позвоночника), а также продолженная активность на ЭМГ околопозвоночных мышц поясничного отдела позвоночника на стороне изгиба. Некоторые специалисты считают, что СПБ может быть диагностирован при выраженном (не менее 10°) боковом изгибе, который полностью исчезает при пассивной мобилизации или в положении лежа на спине. Сгибание в одну сторону очень часто встречается в поздних стадиях БП. Сколиоз при БП более распространен, чем в общей популяции пожилых людей, его частота находится в диапазоне от 8,4 до 90,5% при паркинсонизме и от 8,5 до 60% при БП.
У большинства пациентов в ранних стадиях не наблюдают какого-либо бокового изгиба позвоночника. СПБ может развиваться длительно (вначале без явных симптомов и затем с постепенным ухудшением) или с подострым началом, за которым следует быстрое ухудшение в течение нескольких месяцев. Сначала становится заметна тенденция к наклону в одну сторону при сидении пациента на стуле, а несколько позднее — боковое сгибание во время ходьбы. При прогрессировании деформации у пациентов могут появляться болевой синдром, диспноэ или неустойчивость, которая приводит к падениям.
Во время обследования пациент сидит, стоит или идет непроизвольно наклоняясь постоянно в одну сторону. Может быть нарушено восприятие вертикального положения, и при просьбе выпрямиться пациенты полагают, что они уже сделали это; следовательно, активное движение для приведения пациента в положение по средней линии может вызывать ощущение потери равновесия.
Существуют разногласия по поводу того, направлен ли боковой изгиб туловища у пациентов (как при СПБ, так и при сколиозе) в ту сторону, где преобладает выраженность характерных для паркинсонизма симптомов, или в противоположную. Большинство исследователей пришли к выводу, что у пациентов существует тенденция к наклону в сторону, противоположную стороне, и только некоторые авторы не выявили связи между направлением изгиба и латерализацией БП.
Диагноз СПБ можно установить клинически на основании наличия бокового изгиба туловища, который может быть скорректирован при помощи пассивной мобилизации или в положении лежа на спине. Для диагностики и количественной оценки степени сколиоза необходимо проведение визуализационного исследования позвоночника с определением угла Кобба. Как и в случае антеколлиса, есть сообщения, что развитие СПБ может быть побочным эффектом приема лекарственных средств. Первоначально считали, что он развивается вторично при приеме блокаторов дофамина, но в более поздних работах отмечено, что развитие СПБ находится в тесной временной связи с изменениями в дофаминергической терапии (как введение нового лекарственного средства, так и повышение дозы препарата, который уже принимает пациент). Обобщенные критерии для определения варианта постуральной деформации представлены в таблице №8.

Дебют болезни Паркинсона.
При дебюте заболевания клинические проявления имеют следующие особенности:
1. Проявления заболевания, как правило одностороннего характера;
2. Чаще симптомы заболевания развиваются в верхней конечности.
3. Классическими симптомами дебюта заболевания являются: скованность, замедленность, в т.ч. изменение почерка, «подтягивание» руки при ходьбе, неловкость при выполнении мелких движений.
4. Первым симптомом может стать односторонняя боль в плечевом суставе, а также боли в шейном и поясничном отделах позвоночника;
5. Чувство слабости и онемения в руке или ноге;
6. «Приволакивание» нижней конечности с одной стороны при ходьбе;
7. Замедленность ходьбы (по сравнению с исходным уровнем);
8. Затруднение при одевании (рукав одежды или обувь с одной стороны).
Ранние стадии болезни Паркинсона.
На ранних стадиях БП основными клиническими проявлениями становятся: нарушения обоняния, вегетативные нарушения (дисфункция желудочно-кишечного тракта (ЖКТ), мочеиспускания, половой функции, потоотделения, постуральная гипотензия, себорея), аффективные нарушения, нарушения сна, чувствительные нарушения.
Обонятельные нарушения.
Уже на самых ранних стадиях БП характеризуется развитием обонятельного дефицита, при этом обонятельные нарушения могут развиваться за несколько лет до появления двигательных расстройств. Первые публикации по обонятельному дефициту при БП появились в 1975 году, когда было описано повышение порога обоняния у 22 пациентов с клиническим диагнозом БП при вдыхании банан амилацетата. Последующие исследования подтвердили наличие более чем у 50% пациентов с БП повышенного порога при вдыхании амилацетата. В целом, среди пациентов с БП обонятельные нарушения выявляются в 70–90% случаев, а по данным Lotsch с соавт. (2008) — даже в 99% случаев. При этом обонятельные нарушения могут не ощущаться самим пациентом, поэтому для их выявления принципиальным является проведение специального тестирования. После возникновения «субклинических» обонятельных нарушений через 2–7 лет у пациентов развиваются моторные симптомы БП. Показано, что среди неврологически здоровых лиц с выявленным обонятельным дефицитом, как минимум у 10–13% в будущем развивается БП. Лица со сниженной функцией обоняния имеют более высокий риск БП, либо выявления телец Леви на аутопсии: в популяционном исследовании PRIРS (Prospective validation of Risk factors for the development of Parkinson Syndrome) относительный риск развития БП среди лиц с гипосмией за три года составил 3,9%, а по данным проспективного исследования Гонолулу, риск развития БП у неврологически здоровых людей с гипосмией возрастает в 5 раз. У ближайших родственников больных БП гипосмия повышает риск развития заболевания в ближайшие 2 года на 10–20%. Показано, что снижение обоняния характерно для БП и болезни диффузных телец Леви, но не для других паркинсонических синдромов, таких как прогрессирующий надъядерный паралич и другие.
Точность оценки степени и характера гипосмии значительно повышается при использовании специальных тестов — UPSIT (Пенсильванский тест), Sniffin’ Sticks и др.
Как уже сказано ранее, моторные проявления при БП начинаются при гибели не менее 60% дофаминэргических нигральных нейронов, тогда как для обонятельной дисфункции подобные корреляции установить сложнее. В целом, не выявлено зависимости гипосмии от стадии болезни: так, на развернутых стадиях БП количественная оценка дефицита обоняния, по данным многих авторов, не коррелировала с возрастом, тяжестью состояния (включая уровень моторных и когнитивных нарушений), длительностью заболевания и проводимой терапией. Однако есть и другая точка зрения: используя Sniffin’ Sticksтест, Daum et al. (2000) нашли отрицательную корреляцию между уровнем дискриминации запахов и тяжестью БП. Аналогичным образом, Tissingh et al. (2001) выявили отрицательную корреляцию между обонятельной дискриминацией и стадией заболевания по шкалам UPDRS и Hoehn-Jahr. Hawkes с соавт. (1993) с помощью UPSIT-теста обнаружили возрастную линейную регрессию обоняния при БП, что свидетельствует об объединенном эффекте понижения обоняния как по возрасту, так и по развитию БП. Эти данные показывают сложность интерпретации гипосмии у пожилых пациентов с БП. Действительно, способность идентификации запахов начинает уменьшаться уже с 36 лет, а между 56 и 80 годами 50% лиц имеют тот или иной дефицит обоняния. Deeb et al. (2006) сообщили о существенной корреляции между суммой баллов в UPSIT-тесте и моторными нарушениями уже в ранних стадиях БП. Это наблюдение, наряду со многими другими, подчеркивает ассоциацию обонятельных и моторных нарушений при БП. Согласно данным Sniffin’ Sticks-теста, у пациентов с БП ольфакторная дисфункция проявляется в виде ухудшения всех трех показателей, но наиболее значимым является нарушение идентификации запахов, при этом, с удлинением срока идентификация запахов остается неизменной, а вот значения дискриминации запахов ухудшаются. В отличие от этих данных, Lotsch с соавт. (2008) при проведении Sniffin’ Sticks-теста сделали вывод, что наиболее показательна для БП сумма всех трех изучаемых параметров в целом, менее значим пороговый тест, еще менее значимы идентификация и дискриминация по отдельности. При исследовании гипосмии в качестве биомаркера БП интересны работы, оценивающие прогностический потенциал ольфакторных нарушений непосредственно для самого течения БП. В своей работе Stephenson с соавт. (2010) показали связь между выраженностью гипосмии и повышенным риском определенных осложнений БП, а именно, когнитивных нарушений и зрительных галлюцинаций. Для этого с помощью UPSIT-теста были обследованы 100 пациентов с БП, длительность от начала симптомов БП до тестирования обоняния составила в среднем 3,6 лет. При повторном обследовании спустя 6,8±4,6 лет оказалось, что у 37% больных развились зрительные галлюцинации, у 38% — когнитивные нарушения, у 66% — дискинезии, а у 65% появились падения. Сопоставление этих осложнений с данными UPSIT показало, что выраженная гипосмия является прогностически неблагоприятной в отношении развития когнитивных нарушений и зрительных галлюцинаций. При этом гипосмия не является предиктором моторных осложнений БП. Был сделан вывод, что нарушения обоняния отражают, прежде всего, экстранигральную патологию, а не стриатонигральную дисфункцию. Это согласуется с постадийным развитием БП, в котором обонятельные луковицы представляют собой промежуточный этап на пути распространения телец Леви к коре больших полушарий. Сходные данные получены Baba et al. (2012): авторы показали, что выраженная гипосмия — предиктор развития деменции при БП по результатам 3-х-летнего наблюдения. Таким образом, поскольку гипосмия может быть непосредственным, прогностически важным маркером инвалидизирующих нейропсихиатрических осложнений, ее диагностика имеет значение для выстраивания особой стратегии лечения БП.
Снижение обоняния при БП объясняется, в первую очередь, патоморфологическими исследованиями, в которых показано, что обонятельные луковицы поражаются на начальных стадиях еще до вовлечения черной субстанции в процесс нейродегенерации. Обонятельная луковица содержит около 20 медиаторов, включая дофамин. И если моторный дефицит при БП связан с дофаминэргической денервацией стриатума, то в обонятельной луковице при БП (во всяком случае, в дебюте заболевания) значимого дефицита дофамина нет. Иными словами, у пациентов имеет место функциональная аносмия, которая подтверждена исследованиями Herting et al. (2008). При проведении повторных обонятельных тестов через 3–6 лет обнаружилось, что ольфакторная функция нестабильна, а ее изменения имеют сложный нелинейный характер. Объяснение обонятельной дисфункции при отсутствии дефицита дофамина в обонятельной луковице найдено Huismann et al (2004). Авторы обнаружили увеличение дофаминэргических нейронов в луковице у больных БП, что вызывает изменения в расшифровке ольфакторной информации. В этом случае ольфакторный дефицит может быть связан с увеличением ингибирования дофаминэргических нейронов в луковице, что способствует гипосмии или функциональной аносмии.
Помимо нарушения дофаминергической медиаторной системы, в генезе обонятельных нарушений при БП имеет значение изменение холинергической активности в гиппокампе, миндалине и неокортексе. В исследовании Bohnen et al. (2010) с помощью обонятельного теста UPSIT и позитронно-эмиссионной томографии (ПЭТ) с [11C] метил-4-пиперидинил пропионатом выявлена была достоверная позитивная связь между активностью холинэстеразы в лимбической системе и уровнем нарушения обоняния. При этом снижение обоняния по шкале UPSIT больше коррелировало с уровнем активности холинэстеразы в лимбической системе, чем с активностью моноаминергической иннервации в стриатуме. Поскольку на сегодня имеется уже достаточно данных о наличии обонятельных нарушений в премоторной стадии БП, последние исследования обоняния при нейродегенеративных заболеваниях направлены на отработку алгоритма для дифференциальной диагностики и раннего выявления так называемой группы риска — лиц, имеющих высокую предрасположенность к развитию БП. Так, например, обонятельное тестирование входит в скрининговые популяционные программы PARS (Parkinson Associated Risk Syndrome), PRIPS (Prospective validation of Risk factors for the development of Parkinson Syndrome) и др. Работы группы S. Boesveldt показывают, что расширенные обонятельные тесты не увеличивают диагностическую точность при БП по сравнению с одиночными тестами. Очевидно, идентификационного теста из 16 предметов, входящего в Sniffin’ Sticks-тест, достаточно, чтобы уловить ольфакторные нарушения при его использовании.
Нарушения психоэмоциональной сферы.
Депрессия — наиболее распространенный симптом при БП. До 45% всех пациентов с БП имеют клинически значимую депрессию. F. Nilsson и соавт. установили, что пациенты с депрессией имеют больший риск развития БП, чем пациенты с остеоартритом и сахарным диабетом. Другое ретроспективное исследование выявило, что прижизненный диагноз депрессии до постановки диагноза БП встречался более чем в 2 раза чаще при сравнении с контрольной группой. Выявление депрессии имеет важное значение, так как она является наиболее значимым фактором, влияющим на качество жизни пациентов с БП. Выявление депрессии при БП осложнено тем, что клиническая картина может включать, как ранние когнитивные нарушения, так и акинетическую симптоматику паркинсонизма, например гипомимию, брадифрению, апатию и др. В патогенезе депрессии играет роль дисфункция дофамин-, серотонин- и норадренергических путей лимбической системы.
Тревожные расстройства также широко распространены при БП и могут быть ее преклиническим фактором риска. По данным различных исследований, до 40% пациентов с БП имеют различные панические расстройства. Спектр тревожных расстройств при БП включает панические атаки, простые и социальные фобии, агорафобию, генерализованные тревожные и недифференцированные тревожные расстройства, фобические, а также обсессивно-компульсивное нарушения. Тревога может быть дофаминзависимым явлением, являясь частью эпизодов «конца дозы» (периоды ухудшения симптомов в конце действия дозы дофаминергического препарата), часто в виде панических атак. В таких случаях она отвечает на коррекцию дофаминергической терапии, направленной на предотвращение подобных эпизодов. Тревога, ассоциированная с депрессией, в некоторых случаях может отвечать на дофаминергическое лечение, но у части пациентов требует специальной коррекции.
Апатия является отдельным симптомом БП, который может возникать вне зависимости от наличия депрессии, сонливости и утомляемости, хотя иногда сочетается с депрессией или тревожным расстройством. Пациенты с БП имеют более высокий уровень апатии по сравнению с пациентами с остеоартритом с аналогичной степенью дезабилитации. Хотя в основе апатии, вероятно, лежит дофаминергическая дисфункция, не исключается вовлечение и других нейротрансмиттерных путей, и ее не всегда удается устранить дофаминергическими препаратами.
Нарушения сна. Диссомния при болезни Паркинсона.
Практически все пациенты с БП имеют нарушения сна уже на ранних стадиях заболевания в виде трудностей засыпания, частых пробуждений, ночной скованности, болезненных дистоний, периодических движений конечностей во сне, выраженной дневной сонливости и др. Причиной их возникновения предположительно является дегенерация центральных стволовых структур и таламокортикальных путей. Нарушение REM-фазы сна наблюдается у 1/3 пациентов с БП, представляя собой парасомнию, с потерей нормальной атонии скелетной мускулатуры, что позволяет пациенту физически осуществлять свои сны. Сон сопровождается вокализациями (разговор, крик) и движениями (подергивания рук и ног, падения с кровати, нападение), которые соответствуют содержанию снов, обычно носящих негативный и яркий характер. Более чем у 30% пациентов с БП имеются полисомнографические критерии нарушения REM-фазы сна, а более чем у 50% — его эпизоды без атонии. Нарушение REM-фазы сна может задолго предшествовать развитию двигательного паркинсонизма у пациентов с БП. Наблюдение за 29 пациентами с идиопатическим нарушением REM-фазы сна показало, что через 4 года БП развилась у 39% пациентов, а через 7 лет — у 60%. У пациентов с идиопатическим нарушением REM-фазы сна имеется симметричное снижение захвата дофамина в стриатуме, что может свидетельствовать о преклинической БП. Вероятно, нарушение REM-фазы сна может возникать по причине дегенерации ядер нижних отделов ствола, обеспечивающих нормальную атонию в REM-фазе сна (педункулопонтинное ядро, голубоватое место, ретрорубральное ядро), что характерно для стадий I и II по Брааку.
Выраженная дневная сонливость наблюдается у 50% пациентов с БП, значительно влияя на качество их жизни. Сонливость вызывает нарушение концентрации внимания, ухудшение памяти, может явиться причиной дорожно-транспортных происшествий и травм. Причиной сонливости может быть заболевание само по себе, фрагментация ночного сна, побочные эффекты антипаркинсонических препаратов. У ряда пациентов прием дофаминовых агонистов может вызвать эпизоды внезапной сонливости. Предполагается существование вторичной нарколепсии без катаплексии при БП, связанной с дегенерацией гипокретиновых (орексиновые) нейронов гипоталамуса.
Вегетативные нарушения при болезни Паркинсона.
Вегетативные нарушения включают ортостатическую гипотензию, дисфункцию мочевого пузыря, половые нарушения, запоры, гипергидроз и др. В основе их развития лежит дегенерация вегетативных центров — дорсального ядра блуждающего нерва, двоякого ядра, вегетативных центров продолговатого мозга и др. Вегетативные нарушения широко распространены на всех стадиях БП. Так, ортостатическая гипотензия имеется у 30% больных, задержки мочеиспускания — у 32%, запоры — у 36%. Снижение систолического артериального давления при ортостатической пробе более чем на 20 мм. рт. ст. выявлено у 58% пациентов с БП, а у 20% — ортостатическая гипотензия была симптоматической и коррелировала с длительностью БП и приемом дофаминергических препаратов. Возможна ранняя денервация сердца при БП, обусловленная накоплением αSyn.
Запор является одним из наиболее распространенных немоторных симптомов БП и часто предшествует развитию заболевания. Распространенность запоров у пациентов с БП достигает 60% по сравнению с контролем (6—33%). Показано, что через 10 лет после начала запоров риск развития БП в 3 раза выше по сравнению со здоровыми. Возникновение запоров еще на I стадии по Брааку может объясняться поражением дорсального ядра блуждающего нерва. В патологический процесс вовлекается также сплетение Ауэрбаха с симпатической денервацией кишечника. Гастропарез при БП наблюдается редко.
Нарушения мочеиспускания при БП включают императивные позывы и учащенное мочеиспускание, никтурию, неполное опорожнение мочевого пузыря, недержание мочи и др. Наиболее распространена гиперрефлексия детрузора, в то время как его пониженная активность встречается реже. Гиперактивность детрузора проявляется никтурией с или без учащенных позывов в дневное время, а недержание мочи является признаком только поздних стадий БП. Выявлены пародоксальные сокращения мышц антагонистов уретрального сфинктера, коррелирующие с нарушением опорожнения мочевого пузыря в период «выключения».
Наиболее распространенным нарушением половой функции у 2/3 пациентов является эректильная дисфункция. Больные отмечают снижение либидо, затруднения в достижении оргазма, в то время как пациенты с длительным течением заболевания имели увеличение сексуальных фантазий.
Болевой синдром при болезни Паркинсона.
После исключения вторичных причин боли (мышечно-скелетные синдромы, нейропатическая боль) распространенность первичных сенсорных симптомов при БП достигает 40—50%. Сенсорные симптомы описывались пациентами, как покалывание, жжение, похолодание, ощущение жара и боли. Боль может возникать в рамках двигательных флюктуаций, ранней утренней дистонии. Возможна глубокая висцеральная боль, связанная с ретроперитонеальным фиброзом на фоне приема эрготаминовых агонистов. Боль также может быть премоторным симптомом БП. Односторонняя проксимальная спонтанная боль в конечности, особенно на стороне начала и наибольшей выраженности заболевания, является одним из распространенных симптомов БП. Предполагается, что причиной боли при БП является поражение парабрахиального ядра, голубоватого пятна, вторичной соматосенсорной и поясной коры.
Развернутые и поздние стадии болезни Паркинсона.
На развернутой стадии БП к вышеперечисленным клиническим симптомам присоединяются когнитивные и психотические нарушения. Развернутые и поздние стадии характеризуются не только количественным нарастанием, но и качественным изменением симптомов.
Кроме того, на развернутой стадии БП клинически значимыми симптомами могут становиться:
1. Дыхательные нарушения, в т.ч.:
— Гипокинезия и утомляемость дыхательных мышц;
— Дисфункция мышц верхних дыхательных путей;
— Респираторная апраксия;
— Обструктивные или центральные апноэ во сне;
— Нарастание в период «выключения».
2. Сенсорные нарушения, в т.ч.:
— Ощущения покалывания, жжения, зуда, онемения, болей;
— Отсутствие зон гипо- или гиперестезии;
— Нарастание в период «выключения».
3. Хроническая усталость — состояние крайнего утомления, слабости, истощения, упадка физических и психических сил, наступающих в результате выполнения привычной для пациента нагрузки и ограничивающее его функциональную активность.
4. Немоторные флюктуации, в т.ч.:
— Тревога — 49%
— Гипергидроз — 48%
— Дизестезия — 48%
— Усталость — 42%
— Дисфория — 37%
— Кардиалгии — 29%
— Нарушения мочеиспускания — 26%
— Одышка — 10%
— Боль — 18%
5. Моторные флуктуации, в т.ч.:
— Феномен истощения конца дозы, т.е. постепенное ослабление эффекта к концу действия дозы леводопы в виде нарастания симптомов паркинсонизма в утренние часы или к моменту приема следующей дозы;
— Исчезновение или значительное уменьшение симптомов паркинсонизма после приема очередной дозы;
— Цикличность, предсказуемость нарастания и уменьшения симптомов.
— Феномен «включения» — «выключения». Резкий переход от состояния компенсации симптомов к обездвиженности. Нарастает тяжесть периодов «выключения». Сокращается длительность периодов «включения». Ночная и утренняя акинезия.
— Отложенное «включение». Отложенное «включение» — наступление эффекта через 60 и более минут после приема леводопы. Эпизодическое отсутствие эффекта принятой дозы. Частая причина: несоблюдение режима приема по отношению к еде (особенно богатой белками), нарушение перистальтики желудочно-кишечного тракта (ЖКТ), прием леводопы замедленного высвобождения.
— Отсутствие «включения».
— «Йо-йоинг» — непредсказуемость развития периодов «выключения» и «включения». Спонтанно или на фоне случайных причин (например, стресс) внезапное «выключение». Внезапное улучшение крайне редко.
6. Дискинезии, в т.ч.:
— Дискинезии пика дозы. Хореоформный или быстрый дистонический гиперкинез (лицо, шея, туловище, конечности). На развернутых и поздних стадиях сопровождают весь период «включения». Причина: сужение терапевтического окна допамина (снижение порога развития дискинезий).
— Дискинезии плато дозы. Хореоформный или быстрый дистонический гиперкинез (лицо, шея, туловище, конечности). На развернутых и поздних стадиях сопровождают весь период «включения». Причина: сужение терапевтического окна допамина (снижение порога развития дискинезий)
7. Двухфазные дискинезии:
— Дистонии «выключения». Фокальная болезненная дистония, чаще в нижних конечностях, реже генерализованная дистония или акатизия.
Моторные флуктуации и дискинезии:
— определяют тяжесть состояния и качество жизни пациента на развернутых стадиях БП;
— встречаются в подавляющем большинстве случаев развернутых стадий БП (30—95% в зависимости от длительности болезни);
— коррекция моторных флуктуаций и дискинезий — основа лечения пациента на развернутых стадиях БП.
Частота моторных флуктуаций и дискинезий:
2 года от начала лечения леводопой: феномен «истощения конца дозы» более 50%, дискинезии — 46%, «вкл — выкл» — 10%;
5 лет: флуктуации и дискинезии 22% пациентов;
БП до 5 лет: флуктуации — 8%, дискинезии — 4%;
БП более 5 лет — 50%, дискинезии — 28%;
БП более 10 лет — флуктуации 75—85%;
БП 15 лет — дискинезия 94%, истощение дозы — 96%.
Когнитивная дисфункция.
Когнитивные нарушения могут наблюдаться уже на ранних стадиях БП, проявляясь нарушением исполнительных функций и зрительно-пространственного дефицита. До 40% пациентов с БП имеют деменцию, что в 6 раз выше, чем в контрольной группе, у 84% она развивается через 15—18 лет от начала заболевания. Клинические проявления деменции при БП включают брадифрению, нарушения зрительно-пространственного гнозиса, флюктуации внимания, расстройства личности и настроения, галлюцинации и психоз, однако речь и праксис остаются преимущественно сохранными. Деменция связана с ухудшением эффективности дофаминергического ответа и, следовательно, прогноза заболевания. Несмотря на наличие в кортикальных и субкортикальных структурах телец Леви, основной причиной развития когнитивных нарушений является гибель холинергических нейронов в базальном ядре Мейнерта, причем объем гиппокампа при БП и болезни Альцгеймера уменьшен в аналогичной степени.
Психотические нарушения.
Наличие психотических симптомов значительно ухудшает прогноз БП и увеличивает смертность. Клинический спектр психоза при БП включает зрительные иллюзии, галлюцинации, параноидный галлюцинаторный психоз, бред и другие симптомы. Малые или экстракампинные галлюцинации представляют собой феномены «присутствия» и «прохождения», когда у больного возникает ощущение присутствия некоего существа (человек или животное) за спиной в комнате или его прохождения по периферии поля зрения. До 40% пациентов с БП имеют зрительные галлюцинации, которые обычно носят яркий хорошо оформленный характер, слуховые и обонятельные галлюцинации встречаются реже. Вероятной причиной возникновения зрительных галлюцинаций при БП является дегенерация педункулопонтинного ядра, голубоватого пятна и ядер шва, которая также приводит к развитию поведенческого нарушения REMфазы сна. Факторами риска возникновения галлюцинаций являются когнитивные нарушения и прием препаратов L-ДОФА; возраст, длительность заболевания и депрессия не играют значительной роли.
Все классы антипаркинсонических препаратов способны провоцировать галлюцинации и психоз. Провокация появляется предположительно по причине возникновения фрагментации сна, приводящей к ярким сновидениям, галлюцинациям и делирию. Ранние галлюцинации в ответ на назначение дофаминергической терапии при БП коррелировали с развитием когнитивных нарушений и деменции.
Диагностика болезни Паркинсона
Доклиническая диагностика
В настоящее время известно, что для БП характерна продромальная фаза, однако выявление людей с субклиническими проявлениями БП остается сложной задачей. Результаты патологоанатомических исследований свидетельствуют о том, что на момент постановки диагноза в черной субстанции отмечается выраженная потеря нейронов, а в последующие 4 года происходит почти тотальная гибель дофаминовых окончаний в дорсальной области стриатума. Путем экстраполяции этих данных было рассчитано, что патологические процессы в головном мозге начинаются за 5–10 лет до появления первых клинических симптомов и постановки диагноза, поэтому перспективным представляется поиск предикторов БП. Среди возможных предикторов БП выделяют: поведенческое расстройство фазы быстрого сна (ПРФБС), идиопатическую аносмию и моногенные мутации, тесно связанные с БП.
ПРФБС характеризуется отсутствием мышечной атонии во время фазы быстрого сна, из-за чего во сне могут возникать вокализации или сложные двигательные акты. Расстройство, как правило, манифестирует у мужчин старше 50 лет (средний возраст 50–65 лет). ПРФБС тесно связано с БП и другими синуклеинопатиями, такими, как деменция с тельцами Леви и мультисистемная атрофия, и часто впервые выявляется при этих заболеваниях у людей с отсутствием расстройств сна в анамнезе. Кроме того, почти у всех людей с ПРФБС впоследствии развивается одно из трех заболеваний. ПРФБС как изолированное расстройство и как продромальная фаза БП сочетается с объективными и субъективными признаками моторного и немоторного дефицита, включая нарушение баланса равновесия, изменение походки и другими большими и малыми признаками двигательной заторможенности.
Хроническая аносмия или гипосмия может быть обусловленной рядом состояний: врожденных, посттравматических, постинфекционных, идиопатических, или быть связанной с нейродегенерацией. Аносмия — нередкое явление, оно встречается в 20% популяции. Аносмия характерна для большинства пациентов с БП. У родственников лиц с БП, не имеющих нейропсихических или установленных обонятельных расстройств, нарушения обоняния свидетельствуют о повышенном риске развития БП в течение 2 лет. Потеря обоняния ассоциирована с 5-кратным повышением риска БП в течение 4 лет наблюдения, при поправке на возраст и другие факторы, играющие роль в развитии БП (курение сигарет, потребление кофе, запоры).
В исследовании факторов риска БП (The Parkinson At-Risk Study, PARS) проводился поиск признаков продромальной фазы заболевания. Были обследованы 669 взрослых человек старше 50 лет с гипосмией, как основным продромальным признаком БП, и 4330 человек с интактным обонянием. В группе с нарушением обоняния чаще встречались запоры (21% против 16% в группе с интактным обонянием), тревога (в психическом статусе у 19% против 14%, как черта личности у 23% против 17%) и депрессия (19% против 11%). Признаки ПРФБС также были более распространены у людей с гипосмией (12% против 7% или 3% против 1% для непроизвольных движений разной интенсивности). В другом аналогичном исследовании около 700 человек в возрасте 50–85 лет с признаками продрома (нарушение обоняния, депрессия или ПРФБС) осматривались дважды в год. Выраженные различия были отмечены в частоте возникновения запоров (7% в группе аносмии, 22% в группе ПРФБС и 25% в группе депрессии), нарушений сна, отличных от ПРФБС (34%, 65% и 53%, соответственно), зрительно-пространственного восприятия (2,2%, 12% и 14%, соответственно), ортостатической гипотензии (13%, 33% и 25%) и когнитивных нарушения (брадифрения: 24%, 36%, 46%, запоминание слов: 37%, 60%, 53%). Таким образом, наиболее тесные связи с остальными признаками были выявлены для ПРФБС.
Методы исследования обонятельного анализатора.
В Европе с 1995 года cертифицирован Sniffin’ Sticks test (Сниффин Стикс тест, ССТ). Сейчас его используют в Германии, Австрии, Швейцарии, Италии. Тест является многоразовым, портативным, функционирует 6–12 мес. Включает скрининг и экстендид (расширенный) тесты (рис. 9).
ССТ состоит из трех испытаний:
1. Определение порога обоняния, чувствует ли пациент запахи. Порог — это та минимальная концентрация запаха, которую ощущает пациент. В 16 пронумерованных карандашах находится н-бутанол в разных концентрациях от 1 до 16 по убыванию интенсивности запаха. В триплет входит один карандаш с запахом, два без. Тест начинается с того, что испытуемому предлагают определить, чувствует ли он запах в карандаше N1 с самой высокой концентрацией н-бутанола. Затем подносят карандаш N16, 15, 14… и т. д. до правильного определения карандаша с запахом. Карандаши в триплете меняют местами и проводят повторное исследование. Результат считается положительным, когда повторное исследование совпало с предыдущим. Далее проводят то же самое с другой пробиркой с большей интенсивностью запаха и т. д. В тесте должно быть 7 максимальных ответов, по последним 4 из которых выводят среднее значение.
2. Определение дискриминации. Это способность выбрать 2 одинаковых запаха из 3 предлагаемых. Тест состоит из 16 пронумерованных триплетов, каждый карандаш в триплете дается 1 раз. Сумма положительных ответов из 16 является количественным результатом теста.
3. Определение идентификации. Способность определить запах по предложенным 4 наименованиям. Пациенту подносят по 1 карандашу из 16 для вдыхания запаха, перед глазами он имеет 4 названия запахов, один из которых должен выбрать (рис. 10). Результат складывается из суммы положительных ответов на 16 предъявленных запахов.
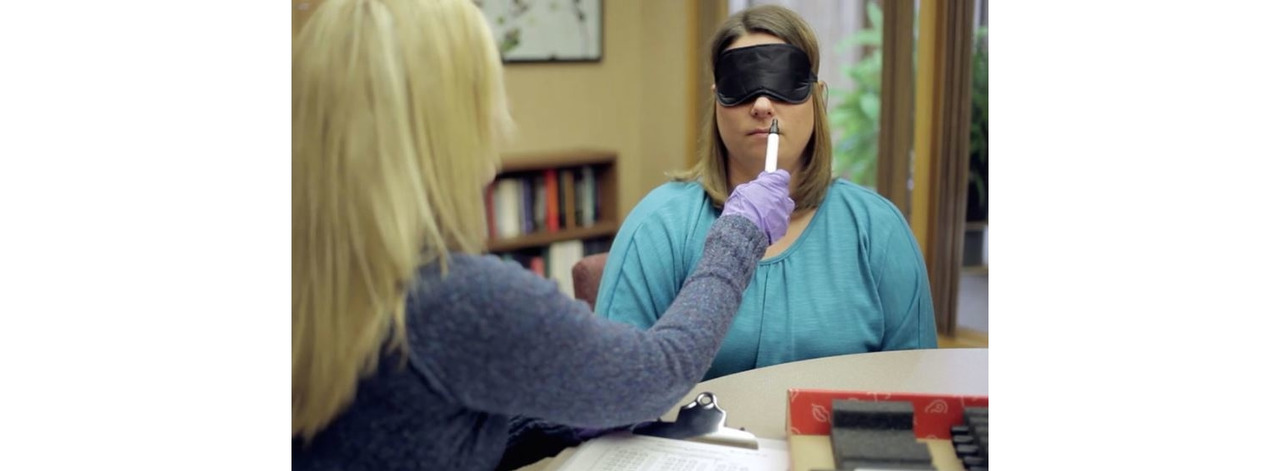
Smell identification test или Пенсильванский тест разработан в 1984 году в Пенсильванском университете (США). Тест Пенсильванского университета позволяет выявить большинство нарушений обоняния и исключить симуляцию расстройств обоняния. Тест содержит 40 образцов различных запахов с четырьмя вариантами ответа каждый. Образцы запаха представляют собой пластинки микрогранул, нанесенные на плотную бумагу (рис. 11). Тест снабжен точным количественным расчетом показателей, свидетельствующих о развитии заболевания. Достоинством теста являются: надежность, низкая себестоимость, простота использования, возможность тестирования в любых условиях, даже самотестирования в домашних и полевых условиях. Тест отличает очень высокая воспроизводимость результатов (r=0,90—0,92).
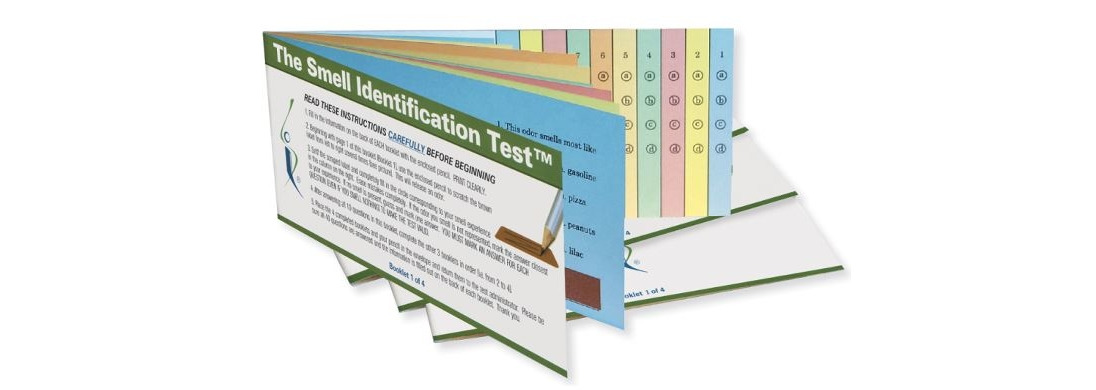
Методы исследования нарушений почерка.
Современные технологии позволяют оценивать параметры почерка по объективным показателям. Специалистами из Университета Хайфы Сарой Розенблюм и профессором Тамаром Вейссом с этой целью был разработан прибор под названием «ComPET». Он состоит из беспроводной электронной ручки и бумаги, наложенной на электронную табличку, на которой человек пишет. Система состоит из двух блоков: для сбора и для анализа данных. Прибор оценивает время контакта ручки с бумагой и время, когда ручка зависает в воздухе, скорость и ускорение, размер букв и промежутки между буквами, степень давления ручки на бумагу и т. д. Специальный софт проводит графический компьютерный анализ. К его разработке были привлечены специалисты-почерковеды. Образцы почерка сохраняются в оцифрованном виде, что позволяет сравнивать их в разных группах и через разные промежутки времени. В случае БП появляется возможность следить за развитием и прогрессированием заболевания.
В эксперименте с участием 40 испытуемых прибор «ComPET» по анализу почерка выявил БП на ранней стадии с точностью 95%. Ранее с помощью этой же методики ученые из Университета Хайфы выявляли детей с синдромом гиперактивности с нарушением внимания, почерк которых имеет характерные особенности. Кроме того, такую систему можно использовать и для коррекции нарушений почерка, в этом случае она работает по принципу биологической обратной связи.
Диагностика на ранних и поздних стадиях болезни Паркинсона
Анамнез, жалобы и клинические проявления.
Диагностические критерии.
Жалобы:
· тремор (мелкое дрожание конечностей, головы) в конечностях, голове. Обычно возникает в покое, уменьшается при попытке двигать конечностями;
· скованность в мышцах — усиливается при повторных движениях (каждое движение выполняется все сложнее);
· нарушение походки (ходьба мелкими шаркающими шажками); · частые падения (возникают из-за развившейся неустойчивости пациента);
· замедленность движений;
· бедность мимики (отсутствие мимики, лицо практически не выражает эмоций);
· ухудшение памяти, мышления;
· эмоциональные нарушения: склонность к ворчливости, подавленное настроение;
· повышенное слюноотделение изо рта.
Анамнез:
· необходимо уточнить в каком возрасте началось заболевание, какие симптомы были его первым проявлением;
· необходимо уточнить, как началось заболевание (постепенно (незаметно) /внезапно, в связи с какими-либо факторами);
· обратить внимание на наличие когнитивных нарушений, депрессии, галлюцинаций;
· выяснить наличие в семейном анамнезе БП/других нейродегенеративных заболеваний (либо их отдельных симптомов, например, тремора) у родственников, наличие в анамнезе повторных травм головы, профессионального/бытового контакта с токсичными веществами;
· в отношении принимаемых в настоящее время лекарственных средств, уточнить наличие сопутствующих заболеваний.
Физикальное обследование.
Неврологический статус:
· гипокинезия (акинезия);
· ригидность;
· тремор в покое, представляющий ритмическое дрожание II, III и противопоставленного им I пальца кисти с частотой 4—6 Гц, напоминающий скатывание пальцами хлебного шарика (по типу «катания пилюль»/«счёта монет»). В начале заболевания тремор односторонний/асимметричный, усиливается на холоде, при эмоциональном напряжении и усталости, ходьбе, движениях в контралатеральной руке. При движении конечности тремор уменьшается/исчезает, во время сна отсутствует. По мере прогрессирования становится двусторонним, присоединяется дрожание стоп, челюсти, языка, век. Редко возможен дебют с асимметричного, одностороннего тремор покоя стоп;
· вегетативные расстройства;
· аффективные нарушения;
· когнитивные дисфункции;
· психотические нарушения.
Гипокинезия:
· замедленностью движений;
· нарушением инициации;
· снижением скорости и амплитуды повторяемых движений;
· гипомимия;
· редкое мигание;
· замедленная речь (брадилалия);
· гипофоничная и монотонная речь;
· дисфагия с затруднением глотания слюны;
· утрата содружественных движений (ахейрокинез);
· шаркающая, короткими шагами походка;
· мелкий почерк (микрография);
· затруднения при поворотах в постели; · замедленность в повседневной активности.
Ригидность:
· скованность/чувство стягивания в шее, нижней части спины, в мышцах руки/ноги (в начале заболевания ригидность носит асимметричный, односторонний характер усиливается при отвлечении внимания/движениях в контралатеральной конечности);
· мышечный тонус вязкий, пластический, монотонный, усиливается при каждом повторном пассивном движении в процессе проверки (феномен «восковой куклы», феномен «свинцовой трубы») толчкообразно меняется (феномен «зубчатого колеса»).
Постуральная неустойчивость:
· нарушение способности удерживать равновесие тела/ходьбе; Нарушение способности удерживать равновесие тела/ходьбе предрасполагает пациента к частым падениям чаще вперед, реже назад при ходьбе, поворотах на месте, вставании с кресла или постели. Для выявления позных нарушений проводят толчковую пробу на пропульсию/ретропульсию. В ранних стадиях БП затрудняются преимущественно тонкие движения в конечностях. Для выявления лёгкой степени гипокинезии можно попросить больного побарабанить пальцами по столу, постучать стопой о пол, быстро сжимать и разжимать кулаки, пронировать и супинировать предплечья. Следует обращать внимание на асимметрию движений, на феномен «истощаемости» (декремент) — замедление движения при его повторении с уменьшением амплитуды.
Немоторные симптомы БП.
1. Вегетативные расстройства, как на ранней, так и, особенно, в развёрнутой стадии: запоры; ортостатическая гипотензия; недержание мочи и кала; эректильная дисфункция; слюнотечение; слезотечение; расстройство терморегуляции; нарушение потоотделения (гипогидроз/гипергидроз); себорея.
2. Сенсорные расстройства в виде ощущения покалывания, онемения, жжения, зуда (50% пациентов); нарушение обоняния (90% пациентов).
3. Психические нарушения (развернутой стадии). · возможно депрессия и тревога (на ранней стадии). · возможно развитие обсессивно-компульсивного синдрома (на поздней стадии).
4. Когнитивные нарушения легкой и умеренной степени выраженности в первые 5 лет отмечаются у большинства больных. Признаки деменции появляется спустя 5 лет и более, крайне редко в первые годы болезни. Расстройства сна — обусловлены как самой БП (пробуждение в ночное время вследствие ригидности и гипокинезии), так и побочным действием лекарств, особенно АДР (дневная сонливость, приступы внезапного засыпания). Психотические нарушения (галлюцинации, иллюзии, бредовые расстройства, нарушение идентификации, делирий) могут возникать у 20—30% больных на любой стадии болезни и в любом возрасте, но чаще у пожилых пациентов с поздней стадией БП, у больных акинетико-ригидной формой и постуральной неустойчивостью в сочетании с деменцией.
Острая декомпенсация БП:
· нарастание основных клинических проявлений паркинсонизма, особенно гипокинезии, ригидности, постуральной неустойчивости;
· нарушение речи (вплоть до анартрии) и глотания;
· усиление моторных флуктуаций и дискинезий;
· психические расстройства (спутанность сознания, галлюцинации, параноидный бред, кататония);
· вегетативная нестабильность (ортостатическая гипотензия, нарушения сердечного ритма, терморегуляции, потоотделения, моторики ЖКТ, мочеиспускания);
· разновидность декомпенсации — акинетический криз, характеризующийся резким нарастанием гипокинезии и ригидности с развитием обездвиженности, анартрии и нарушения глотания, а также акинетико-гипертермический (злокачественный) синдром, для которого, помимо проявлений акинетического криза, характерна гипертермия (гиперпирексия), вызванная дисфункцией гипоталамуса. Сопровождающееся существенным ограничением функциональных возможностей пациента и сохраняющееся более 24 часов, несмотря на продолжение/возобновление привычной для пациента противопаркинсонической терапии.
Алгоритм диагностики паркинсонизма.
В диагностическом алгоритме БП (рис.12) можно выделить два этапа.
Первый этап — установление синдрома паркинсонизма и дифференциальная диагностика его с внешне сходными состояниями, в том числе эссенциальным/дистоническим тремором, аффективными нарушениями (апатия, депрессия, абулия), паратонией, истерией, апраксией ходьбы (лобной дисбазией) при сосудистых поражениях головного мозга/гидроцефалии, гипотиреозом.
Второй этап предполагает установление нозологического диагноза паркинсонизма и дифференциальную диагностику БП с другими заболеваниями, вызывающими этот синдром.
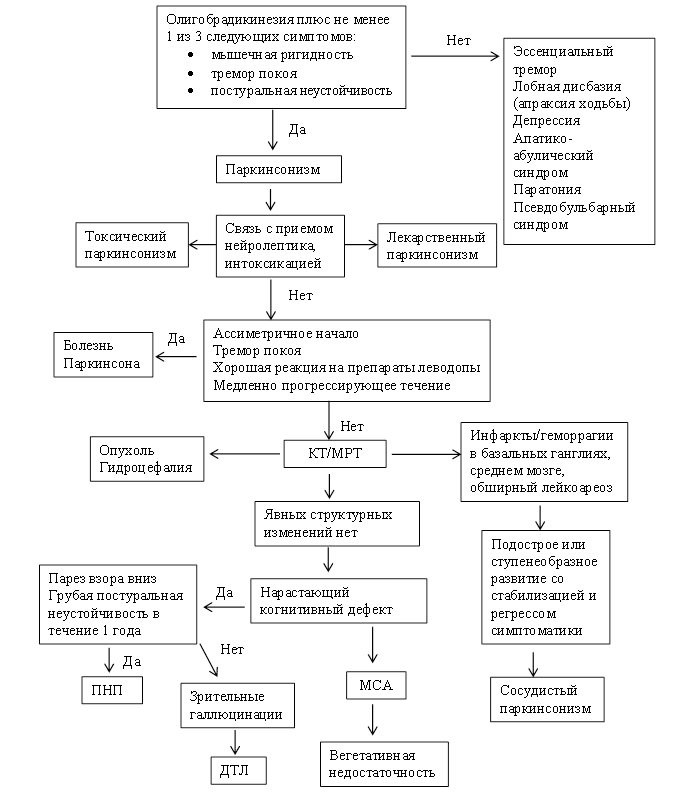
Для клинической диагностики БП используют критерии Банка головного мозга Общества болезни Паркинсона Великобритании. С помощью данных критериев можно установить лишь вероятный диагноз (при наличии не менее трех признаков, относящихся к третьей группе) или возможный диагноз (при наличии менее трех признаков) БП. Достоверный диагноз БП возможен лишь по данным патоморфологического исследования.
Критерии Банка Головного мозга Общества Болезни Паркинсона Великобритании (UK Parkinson’s Disease Society Brain Bank Clinical Diagnostic Criteria)
В настоящее время диагноз БП ставится в соответствии с утвержденными клинико-диагностическим критериям Банка головного мозга общества БП Великобритании (Gibb, Lees, 1988, 2009). Диагностика основана на оценке клинических критериев: наличие синдрома паркинсонизма, отсутствие признаков, исключающих БП и наличие признаков, подтверждающих диагноз. Данные критерии обладают высокой специфичностью (в 98% случаев в дальнейшем подтверждается БП), чувствительность данных критериев приближается к 90%, что означает, что лишь в 10% случаев БП не выставляется при ее наличии.
I этап. Cиндром паркинсонизма.
— Гипокинезия.
+ один из симптомов
— Мышечная ригидность;
— Тремор покоя;
— Постуральная неустойчивость, не связанная с первичными зрительными.
II этап. Критерии исключения болезни Паркинсона вестибулярными, мозжечковыми и проприоцептивными нарушениями.
— Повторные инсульты в анамнезе со ступенеобразным прогрессированием симптомов паркинсонизма;
— Повторные ЧМТ в анамнезе;
— Энцефалит в анамнезе;
— Окулогирные кризы;
— Лечение нейролептиками на момент появления симптомов;
— Семейный характер болезни;
— Наличие длительной ремиссии;
— Односторонняя симптоматика более 3 лет;
— Паралич взора вниз;
— Ранняя быстро прогрессирующая вегетативная недостаточность;
— Мозжечковые знаки;
— Рано развивающаяся деменция с нарушением памяти, речи и праксиса;
— Симптом Бабинского;
— Наличие сообщающейся гидроцефалии на КТ;
— Отсутствие реакции на высокие дозы леводопы;
— Контакт с токсическими веществами, вызывающими паркинсонизм.
III этап. Критерии, подтверждающие диагноз болезни Паркинсона.
— Одностороннее начало;
— Тремор покоя;
— Прогрессирующее течение;
— Сохранение асимметрии симптоматики с преобладанием на первоначально вовлеченной стороне;
— Высокая эффективность леводопы;
— Хореоформные дискинезии, индуцируемые леводопой;
— Сохранение реакции на леводопу в течение 5 лет и больше;
— Течение заболевания 10 лет и больше.
Методы нейровизуализации.
Изменения, выявляемые у пациентов с БП при проведении компьютерной томографии (КТ) и/или МРТ в стандартных режимах являются весьма неспецифичными. Преимущественно по данным нейровизуализации выявляется различной степени выраженности уменьшение объема вещества головного мозга: конвекситальная атрофия корковых отделов мозга, расширение желудочковой системы, которые не являются патогномоничными признаками этой патологии (рис. 13).
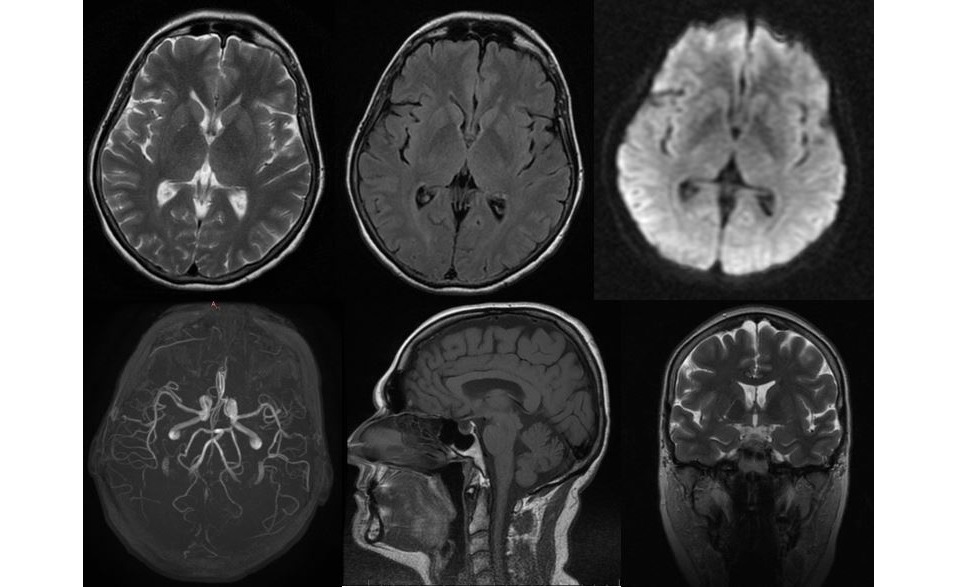
Боковые желудочки мозга не расширены, симметричны (D=S). III-й и IV-й желудочки обычной конфигурации и размеров. Супраселлярная цистерна пролабирует в полость турецкого седла, остальные базальные цистерны не изменены. Субарахноидальные ликворные пространства неравномерно расширены по конвекситальной поверхности в проекции лобных, теменных долей и Сильвиевых щелей. Незначительно расширены периваскулярные пространства Вирхова-Робина по ходу пенетрирующих сосудов. Срединные структуры не смещены. Вертикальный размер гипофиза — до 0,3 см, сохраненная ткань гипофиза имеет обычный МР сигнал.
Более выраженные МР-признаки атрофии отмечаются у пациентов с акинетикоригидной формой заболевания, а также при наличие в клинической картине значительных когнитивных нарушений. Выраженность атрофии нарастает и по мере увеличения тяжести и продолжительности заболевания. Так, при длительности БП до 3 лет атрофия выявляется у трети пациентов, а при длительности свыше 6 лет возрастает более чем в 2 раза и отмечается у 78% пациентов.
Несмотря на то что МРТ в стандартных режимах не выявляет каких-либо патогномоничных признаков при БП, этот метод позволяет исключить другие структурные поражения мозга, сопровождающиеся синдромом паркинсонизма. К таким патологиям относятся опухоль базальных ганглиев, нормотензивная гидроцефалия, сосудистые поражения, изменения сигнала от базальных ганглиев вследствие болезни Вильсона-Коновалова, отравления марганцем и др. МРТ помогает также в дифференциальной диагностике БП с паркинсонизмом вследствие нейродегенеративных заболеваний, при каждом из которых МРТ имеет ряд специфических симптомов: «глаза тигра» (рис. 14).
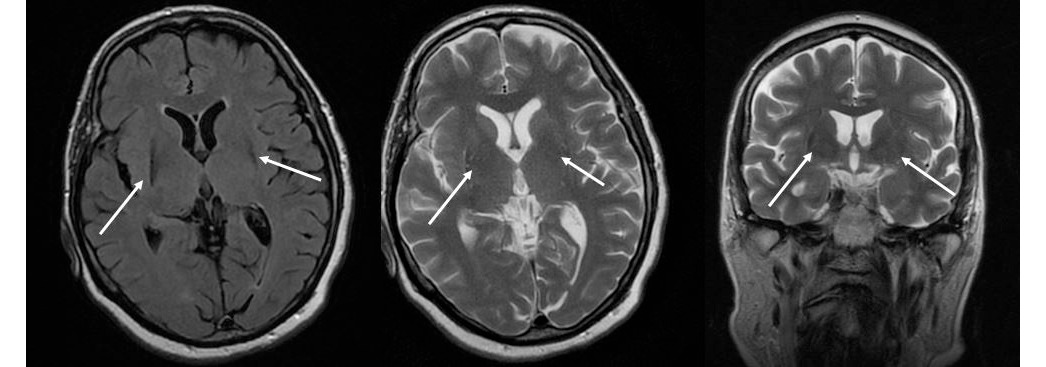
Попытки оценки изменений нейронов в черной субстанции при БП в настоящее время продолжаются с использованием новейших методик нейровизуализации, в том числе МРТ-морфометрии. Этот метод получил распространение только в последнее десятилетие в связи с внедрением в клиническую практику режимов высокого разрешения и появлением метода воксельных преобразований трехмерных данных (VBM-voxel-based morphometry). Оценка объема черной субстанции при МРТ-морфометрии пока не показала значимого уменьшения объема черной субстанции у пациентов с БП, возможно, вследствие трудностей в выделении границ черной субстанции. При БП диффузионная тензорная МРТ выявляет специфичное для данного заболевания снижение фракционной анизотропии в каудальных отделах черной субстанции. По данным D. Vaillancourt, этот признак с 100%-ной специфичностью позволяет дифференцировать БП от группы контроля и может являться дополнительным диагностическим критерием, подтверждающим БП. Полученные D. Vaillancourt результаты согласуются с патоморфологическими посмертными исследованиями у пациентов с БП, выявляющими наибольшую потерю нейронов в вентрокаудальной части черной субстанции. Диффузионно-тензорная МРТ позволяет выявлять микроструктурные поражения белого вещества при наличии когнитивных нарушений и оценивать их по снижению фракционной анизотропии. Методика диффузионно-взвешенной МРТ обладает большей специфичностью по сравнению со стандартными режимами МРТ и позволяет провести дифференциальный диагноз между паркинсонизмом при нейродегенеративных заболеваниях и БП. Программа DWI выявляет увеличение коэффициента диффузии в скорлупе и в области лентикулярных ядер в 80—90% случаев клинически возможной МСА и прогрессирующего надъядерного паралича (ПНП), в то время как у пациентов с БП в этих зонах он остается в пределах нормы.
Депигментация черной субстанции и голубого пятна — значимая патологическая характеристика БП; она связана с потерей нейромеланина, парамагнитные свойства которого приводят к повышению магнитно-резонансного (МР) сигнала на Т1-взвешенных изображениях. Недавними исследованиями было показано, что уменьшение содержания нейромеланина в черной субстанции и голубом пятне при БП может рассматриваться в качестве потенциального биомаркера заболевания. В связи с этим в работе, проведенной в Португалии, оценивалась диагностическая значимость МР-визуализации нейромеланина у пациентов с БП, при этом впервые был использован метод полуавтоматического анализа МР-изображений.
В исследование включались пациенты с БП, диагностированные de novo и не получавшие лечение с длительностью заболевания от 2 до 5 лет. Кроме пациентов с БП была сформирована сопоставимая по возрасту контрольная группа. В исследовании для визуализации нейромеланина использовалась МРТ высокого разрешения 3 Тесла в режиме Т1. Основными исследуемыми переменными были выбраны площадь повышенного сигнала в области черной субстанции, его длина, отношение нейромеланин/средний мозг, полученные с помощью метода полуавтоматической оценки.
Суммарно в исследование были включены 12 впервые диагностированных пациентов с БП и 10 пациентов с длительностью заболевания от 2 до 5 лет. Площадь, длина повышенного сигнала в режиме Т1 от области черной субстанции и отношение нейромеланин/средний мозг были статистически значимо ниже в группе БП по сравнению с контрольной группой, при этом в двух подгруппах заболевания данные показатели существенно не различались. Нейромеланин-чувствительная МР-методика позволяет отличать случаи БП от здоровых лиц с высокой чувствительностью и специфичностью. Полученные данные совпадают с более ранними результатами, свидетельствующими о стабильности содержания нейромеланина в процессе заболевания.
По результатам Stefan T. Schwarz при выполнении МРТ головного мозга на аппаратах повышенной мощности (7 Тесла) и разрешающей способности удается обнаружить структурные изменения тканей мозга в центральной зоне substantia nigra, характерные для людей с БП. В ходе наблюдений было выявлено, что у здоровых людей эта область напоминает изображение хвоста ласточки (рис. 15). У пациентов с БП характерное разделение черной субстанции на две доли «ласточкиного хвоста» пропадает. Для проверки своего метода ученые провели 114 сканирований головного мозга с высоким разрешением. В 94% случаев им удалось поставить точный диагноз. Дальнейшие исследования показали, что «ласточкин хвост» (и его отсутствие) можно разглядеть и на аппаратах мощностью 3 Тесла.
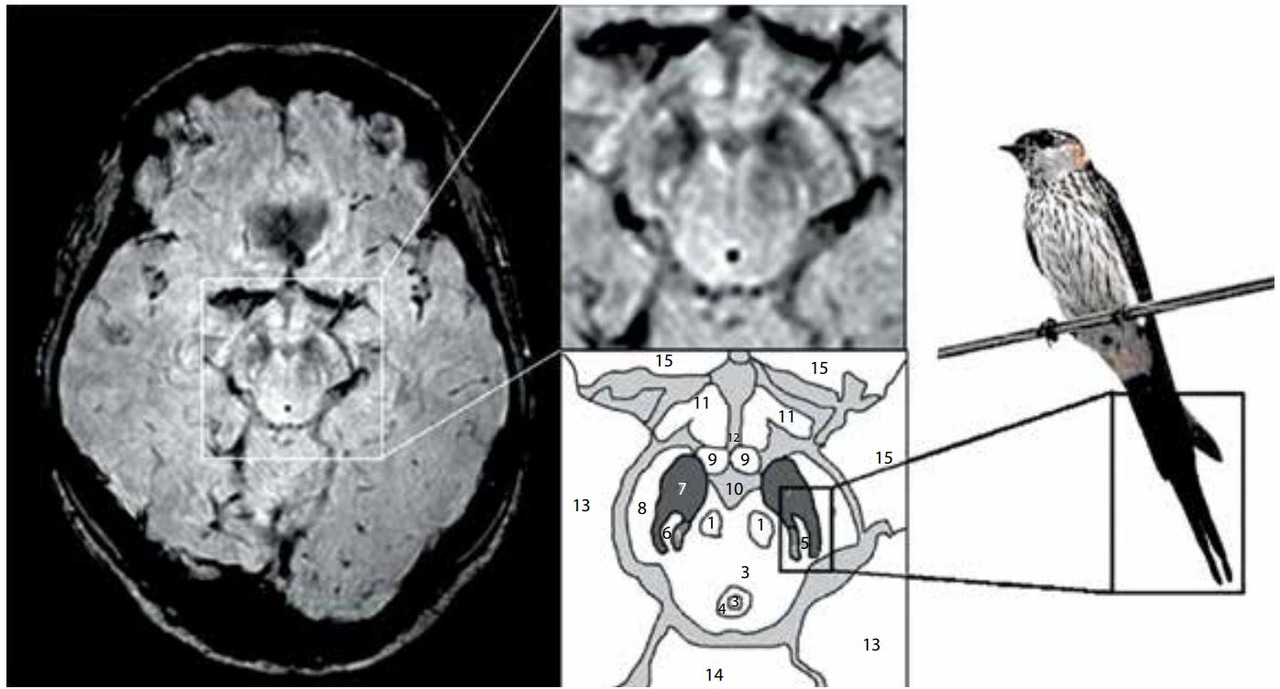
Транскраниальная сонография.
Транскраниальная сонография (ТКС) относится к новым нейровизуализационным методикам, позволяющим выявлять структурные изменения черной субстанции. ТКС представляет собой ультразвуковое исследование вещества головного мозга в В-режиме. ТКС как метод инструментальной диагностики экстрапирамидных заболеваний получил свое развитие в течение последнего десятилетия в связи с появлением нового поколения ультразвуковых аппаратов (рис. 16) с высоким качеством изображения, которое позволило идентифицировать нейроанатомические структуры небольших размеров, патология которых лежит в основе этих заболеваний.
В 1995 г. G. Becker et al. было опубликовано первое описание применения ТКС у пациентов с БП. В работе был выявлен характерный для БП феномен — гиперэхогенность черной субстанции (ГЧС). На сегодняшний день ГЧС является основным, наиболее надежным и воспроизводимым, ультразвуковым биомаркером БП на всех стадиях заболевания.
Физические принципы ТКС, основанные на отражении УЗ-волн от неоднородных структур, обладающих различным акустическим сопротивлением (В-режим), позволяют выявлять характерные изменения черной субстанции, шва мозга, базальных ганглиев, ядер мозжечка, которые невозможно определить иными нейровизуализационными методами с другими физическими принципами получения изображения.
Преимуществами метода ТКС являются неинвазивность, широкая доступность в клинической практике, короткое время и относительно невысокая стоимость исследования, возможность проведения неограниченного количества исследований без риска для здоровья пациента. Кроме того, ТКС не зависит от двигательной активности пациентов, что особенно важно для больных с экстрапирамидными расстройствами и с гиперкинетической активностью. В связи с этим ТКС представляется перспективным инструментальным методом для скрининга и рутинной диагностики заболеваний.
Исследование выполняется через транстемпоральный доступ при расположении датчика в преаурикулярной области. Структуры ствола мозга, базальные ганглии и желудочки визуализируются в трех стандартизированных плоскостях сканирования. Для этих плоскостей разработаны четкие УЗ-ориентиры и определены углы наклона датчика. Для визуализации структур мозга используется фазированный датчик с частотой 2,5 МГц. Устанавливается глубина 140—160 мм, динамический диапазон 45—50 dB. Яркость и контрастность выставляются индивидуально для каждого конкретного случая. Обследование обычно начинают с аксиальной плоскости, параллельной орбитомеатальной линии (линия от наружного края глаза до наружного слухового отверстия). В этой плоскости средний мозг визуализируется в виде «бабочки», окруженной эхогенными базальными цистернами. В плоскости сканирования среднего мозга оцениваются ипсилатеральная область черной субстанции, красное ядро и шов мозга. Особенно тщательно должна быть исследована область черной субстанции в проекции ножек среднего мозга на предмет гиперэхогенности, которая может быть представлена в виде пятна или полосы. Черная субстанция обычно имеет низкую эхогенность и не отличается по УЗ-параметрам от окружающего ее вещества мозга. На настоящий момент считается, что количественная оценка площади ГЧС предпочтительней, нежели качественная оценка интенсивности эхосигнала, так как последняя зависит от ряда изменяемых параметров.
ГЧС признается, если интенсивность УЗ-сигнала от нее превышает таковую от окружающих областей или измеренная площадь превышает нормальные значения, полученные в популяционных исследованиях (более 0,20 см2). В большинстве проведенных независимых исследований ГЧС выявлялась более чем у 85—92% пациентов с БП. Часть исследователей отмечают, что на начальных стадиях БП гиперэхогенность более выражена на стороне, контрлатеральной двигательным нарушениям. В исследовании D. Berg размер ГЧС не коррелировал с выраженностью моторных симптомов и оставался стабильным в течение 5 лет наблюдения, несмотря на прогрессирование симптомов. В связи с этим D. Berg было высказано предположение о том, что ГЧС является биомаркером функциональной несостоятельности черной субстанции и отражает скорее накопление железосвязанных белков, а не гибель дофаминпродуцирующих нейронов. Кроме того, ряд исследований выявил взаимосвязь ГЧС с уровнем ферритина и обратную взаимосвязь с уровнем нейромеланина в черной субстанции. У единичных пациентов с БП и ГЧС выявлены полиморфизмы в генах, участвующих в метаболизме железа, однако ни один из известных на сегодняшний день генов, ассоциированных с БП, напрямую не участвует в метаболизме железа. Несмотря на наличие нигральной дегенерации на аутопсии при МСА и ПНП, этот феномен выявляется при этих заболеваниях только в 25% случаев.
Радиоизотопная компьютерная визуализация: ПЭТ и ОФЭКТ.
ПЭТ с применением специфического лиганда F18-флюородопы позволяет количественно определять дефицит синтеза и хранения допамина в пределах пресинаптических стриарных терминалей. Количество пресинаптичесикх дофаминергических терминалей при БП прогрессивно уменьшается, что выявляется при проведении ПЭТ. При БП происходит уменьшение захвата F18-флюородопы нейронами скорлупы на стороне, противоположной моторным симптомам. Критерий БП — снижение захвата F18-флюородопы в скорлупе на 30% и более. Этот признак, отражающий дегенерацию нигростри-арных нейронов, нередко встречается и при МСА и других нейродегенеративных заболеваниях, но при МСА, ПНП, кортико-базальной дегенерации (КБД) уже на ранней стадии снижается захват этого лиганда и в хвостатом ядре, что не характерно для БП. Оценить состояние постсинаптических дофаминовых рецепторов можно с помощью ПЭТ с лигандом Dj-рецепторов раклопридом. При БП плотность Dj-рецепторов бывает нормальной или повышенной за счет механизмов нейропластичности и незначительно снижается лишь на фоне длительного приема дофаминергических препаратов. При паркинсонизме вследствие других нейродегенеративных заболеваний (МСА, ПНП и КБД) количество постсинаптических дофаминовых рецепторов в полосатом теле уменьшается.
Аналогичные результаты выявляются и при однофотонной эмиссионной компьютерной томографии (ОФЭКТ) с иодобензамидом, которая также позволяет оценить сохранность D2-рецепторов. Данные ПЭТ с Sch23390 указывают на умеренное снижение плотности и Dj-рецепторов при паркинсонизме при других нейродегенеративных заболеваниях. Снижение плотности дофаминовых рецепторов в стриатуме отражает дегенерацию проекционных стриарных нейронов и объясняет низкую эффективность препаратов леводопы при этих заболеваниях. При БП плотность D1-рецепторов уменьшается только на поздних стадиях болезни при относительной сохранности при БП D2-рецепторов. Исходя из этих данных, принято говорить о пресинаптическом паркинсонизме в случае БП и постсинаптическом при МСА, ПНП и других нейродегенеративных заболеваниях. Что касается КБД, ПЭТ и ОФЭКТ выявляют асимметричное снижение поглощения (18F) флуородопы на стороне, противоположной стороне поражения при осмотре, и четкую асимметрию метаболизма в контрлатеральной лобно-теменной коре. Кроме того, при этой патологии отмечается асимметричное снижение числа дофаминовых рецепторов в стриатуме.
Левадопа-тест
Для постановки леводопа-теста больной в течение пяти дней принимает леводопасодержащие препараты (Синемет или Мадопар) в дозе 200—250 мг в три приема на протяжении дня. После чего регистрируют степень изменения (уменьшения) показателей двигательных нарушений с помощью специальной шкалы UРDRS. Если ожидаемый ответ на леводопа-тестирование не наблюдается, то с наибольшей вероятностью заболевание нельзя расценивать как БП.
Дифференциальная диагностика болезни Паркинсона
В некоторых случаях дифференциальная диагностика БП может представлять определенные сложности. К заболеваниям с которыми прежде всего необходимо дифференцировать БП относятся: сосудистый паркинсонизм, лекарственный паркинсонизм, мультисистемная атрофия, прогрессирующий надъядерный паралич и др. При проведении дифференциального диагноза можно воспользоваться алгоритмом предложенным Левиным О. С. (2002 г.) (рис. 17).
Лекарственный паркинсонизм
Обоснование для дифференциальной диагностики: подострое развитие паркинсонизма на фоне приема нейролептика, метоклопрамида, циннаризина, резерпина и др.; сочетание с другими лекарственными дискинезиями; регресс симптомов после отмены препарата.
Критерии исключения диагноза БП: подострое развитие; двусторонний дебют симптомов; преобладание постурального тремора над тремором покоя; сочетание с другими дискинезиями, например с акатизией, стереотипиями, орофациальными дискинезиями; возможность регресса симптомов в течение нескольких недель после отмены соответствующего препарата (иногда регресс симптомов занимает месяцы и даже годы, особенно в пожилом возрасте или после применения препаратов длительного действия).
Множественная (мультисистемная) атрофия (MCA)
Обоснование для дифференциальной диагностики: раннее развитие выраженной вегетативной недостаточности; мозжечковые и пирамидные знаки; антероколлис; возможно улучшение под влиянием леводопы, чаще всего преходящее; атипичные краниоцервикальные дискинезии, вызываемые малыми дозами леводопы; стридор.
Дополнительные обследования: магнитно-резонансная томография (МРТ).
Критерии исключения диагноза БП: Снижение систолического артериального давления (САД) не менее чем на 30 мм рт. ст., либо диастолического артериального давления (ДАД) не менее чем на 15 мм. рт. ст. в вертикальном положении тела. МСА паркинсонического типа:
· быстро прогрессирующий паркинсонизм,
· низкая реакция на леводопу,
· постуральная неустойчивость в первые 3 года,
· мозжечковые знаки,
· дисфагия в первые 5 лет;
· при МРТ: атрофия скорлупы, средней ножки мозжечка, моста или мозжечка,
МСА мозжечкового типа:
· паркинсонизм;
· при МРТ: атрофия скорлупы, средней ножки мозжечка, моста.
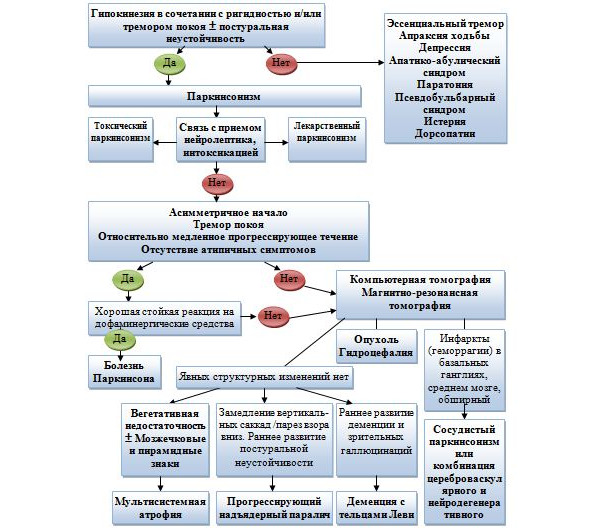
Кортико-базальная дегенерация (КБД)
Обоснование для дифференциальной диагностики: асимметричные акинезия, ригидность, дистония; очаговые нарушения высших корковых функций (апраксия, афазия, игнорирование половины пространства). Феномен «чужой» руки, астереогноз, грубые асимметричные постурально-кинетический тремор и миоклония.
Дополнительные обследования: МРТ либо компьютерная томография (КТ).
Критерии исключения диагноза БП: наличие не менее 3 из следующих 6 признаков:
· акинетико- ригидный синдром, не реагирующий на леводопу;
· феномен «чужой» руки;
· апраксия или нарушения сложных видов глубокой чувствительности;
· фокальная дистония в конечности;
· грубый постуральный или интенционный тремор;
· миоклонии. Отсутствие изменений на КТ/МРТ, но чаще асимметричная атрофия лобной и теменной коры на контрлатеральной симптоматике стороне.
Прогрессирующий надъядерный паралич (ПНП)
Обоснование для дифференциальной диагностики: замедление вертикальных саккад и парез взора вниз; развитие выраженной постуральной неустойчивости на первом году заболевания; грубая дизартрия и дисфагия; ретракция век; симптомы более выражены в аксиальных отделах, чем в конечностях; разгибательная поза, деменция лобного типа.
Дополнительные обследования: МРТ.
Критерии исключения диагноза БП:
Облигатные:
· Неуклонно прогрессирующее течение;
· Начало после 40 лет;
· Парез вертикального взора (вверх или вниз);
· Развитие выраженной постуральной неустойчивости с частыми падениями на первом году заболевания.
Дополнительные:
· Симметричная акинезия или ригидность, более выраженная в проксимальном отделе, чем в дистальном;
· Патологическая установка шеи (ретроколлис);
· Отсутствующая минимальная или преходящая реакция паркинсонических симптомов на препараты леводопы;
· Раннее развитие дисфагии и дизартрии;
· Раннее развитие нейропсихологических нарушений, в том числе двух и более из следующих признаков: апатия, нарушение абстрактного мышления, снижение речевой активности, полевое поведение, эхопраксия или лобные знаки МРТ: атрофия среднего мозга (наиболее частый признак), расширение III желудочка, повышение интенсивности сигнала от верхней ножки мозжечка, бледного шара и красного ядра в Т2-режиме, атрофия лобной и височной коры.
Болезнь диффузных телец Леви (БДТЛ)
Обоснование для дифференциальной диагностики: деменция предшествует развитию паркинсонизма или развивается параллельно с ним; зрительные галлюцинации и другие психотические нарушения в первые годы болезни; флуктуации психических функций, нарушение поведения во сне, относительная резистентность к препаратам леводопы, раннее развитие вегетативной недостаточности.
Дополнительные обследования: МРТ
Критерии исключения диагноза БП:
Основной
· Развитие деменции предшествует развитию паркинсонизма или развивается параллельно с ним, не позднее 1 года с момента появления признаков паркинсонизма.
Дополнительные:
· выраженные колебания внимания и психической активности (на протяжении суток или нескольких дней), иногда с преходящими эпизодами спутанности, которые иногда ошибочно принимают за преходящие нарушения мозгового кровообращения;
· персистирующие зрительные галлюцинации, иногда сопровождающиеся другими психотическими расстройствами, например бредом преследования (они могут быть спонтанными, но иногда провоцируются и противопаркинсоническими средствами);
· нарушение РЕМ-стадии сна (синдром Шенка — разговоры или крики во время РЕМ-стадии сна, моторные выражения снов);
· выраженная гиперчувствительность к нейролептикам;
· нейропсихологическое исследование: деменция смешанного подкорково коркового типа.
· атрофия лобных и височных долей при МРТ.
Сосудистый паркинсонизм
Обоснование для дифференциальной диагностики: наличие признаков цереброваскулярного заболевания (в том числе повторных эпизодов острого нарушения мозгового кровообращения (ОНМК) или последствий нарушения мозгового кровообращения (ПНМК)), преобладание симптомов в нижних конечностях с ранним развитием нарушения ходьбы, отсутствие тремора покоя, пирамидные или мозжечковые знаки; резистентность к леводопе; острое или подострое начало, как правило, в первые 6 месяцев после инсульта, флуктуирующее течение с периодами быстрого ухудшения, длительной стабилизации и спонтанного регресса.
Дополнительные обследования: КТ либо МРТ
Критерии исключения диагноза БП:
диагноз сосудистого паркинсонизма устанавливается при наличии всех следующих критериев:
1) Сочетание гипокинезии не менее чем с одним из следующих трех симптомов: ригидность, тремор покоя, постуральная неустойчивость;
2) Цереброваскулярное заболевание, выявляемое по данным анамнеза и клинического осмотра и/или нейровизуализации (КТ/МРТ);
3) Наличие причинно-следственной связи между паркинсонизмом и цереброваскулярным заболеванием, доказываемое:
· особенностями течения паркинсонизма;
· соответствием между клиническими и нейровизуализационными данными (выявление при КТ/МРТ изменений в стратегических для паркинсонизма зонах — множественных двусторонних ишемических или геморрагических очагов в скорлупе или бледном шаре, а также очагов в лобных долях, среднем мозге или таламусе (с одной или обеих сторон), двустороннего обширного перивентрикулярного и/или субкортикального лейкоареоза)
4) Отсутствие анамнестических или клинических данных, указывающих на иную этиологию паркинсонизма.
Нормотензивная гидроцефалия
Обоснование для дифференциальной диагностики: лобная дисбазия (апраксия ходьбы), недержание мочи, деменция.
Дополнительные обследования: КТ либо МРТ, ликвородинамическая проба (Tap-test).
Критерии исключения диагноза БП:
· КТ/МРТ: резкое расширение желудочков, диспропорциональное по отношению к ширине корковых борозд.
· Улучшение двигательных функций при извлечения 30—50 мл. цереброспинальной жидкости.
Посттравматический паркинсонизм
Обоснование для дифференциальной диагностики: развитие в остром или подостром периоде тяжелой черепно-мозговой травмы (ЧМТ) с последующим стационарным течением либо очень частые повторные ЧМТ (энцефалопатия боксеров) с медленно прогрессирующим течением
Обследования: КТ либо МРТ
Критерии исключения диагноза БП:
· Развитие клинической картины на протяжении нескольких ближайших суток, недель либо месяцев после травмы;
· ЧМТ должна быть достаточно тяжёлой для того, чтобы обусловить значительное повреждение тканей головного мозга (к примеру, сопровождаться длительной потерей сознания, антероградной амнезией);
· При МРТ/КТ должны быть выявлены структурные изменения (очаги ишемии, некроза или кровоизлияний), локализующиеся в области среднего мозга или базальных ганглиев либо признаки тяжёлого диффузного поражения белого вещества больших полушарий мозга.
Эссенциальный тремор
Обоснование для дифференциальной диагностики: тремор в обеих руках при удержании позы или движении, уменьшающийся или проходящий в покое; тремор головы и голосовых связок; отсутствие гипокинезии и ригидности (возможен феномен «зубчатого колеса»! ); длительное доброкачественное течение
Критерии исключения диагноза БП:
· Тремор максимально выражен при удержании позы и при движении;
· Дебют с более или менее симметричного вовлечения рук;
· Частое вовлечение головы и голосовых связок;
· Симптомы паркинсонизма отсутствуют, но возможны легкая атаксия при ходьбе и феномен «зубчатого колеса»;
· Заболевание прогрессирует очень медленно;
· Положительная реакция на алкоголь (2/3 случаев);
· Положительный семейный анамнез (50%).
Гепатолентикулярная дегенерация
Обоснование для дифференциальной диагностики: любой экстрапирамидный синдром, проявившийся в возрасте до 50 лет.
Дополнительные обследования: исследование роговицы с помощью щелевой лампы, определение уровня церулоплазмина, меди в крови и моче, МРТ.
Критерии исключения диагноза БП:
· наличие пигментного роговичного кольца Кайзера — Флейшера (при исследовании щелевой лампой кольцо Кайзера-Флейшера на стадии неврологических проявлений выявляется у 95% больных);
· снижение уровня церулоплазмина в крови (примерно у 10% пациентов уровень церулоплазмина остается в пределах нормы);
· изменение показателей обмена меди: увеличение экскреции меди с мочой (в норме — не более 50 мкг/сут.), снижение общего содержания меди в крови (в норме 0,70—1,45 мг/л), увеличение концентрации в крови свободной (не связанной с церулоплазмином) меди (в норме 0,10—0,15 мг/л);
· повышение интенсивности сигнала от базальных ганглиев и мозжечка на Т2-взвешенных изображениях головного мозга при МРТ (выявляется практически у всех больных с неврологическими симптомами).
МЕДИЦИНСКАЯ РЕАБИЛИТАЦИЯ ПРИ БОЛЕЗНИ ПАРКИНСОНА
Медицинская реабилитация — это комплекс мероприятий медицинского и психологического характера, направленных на полное или частичное восстановление нарушенных и (или) компенсацию утраченных функций пораженного органа либо системы организма, поддержание функций организма в процессе завершения остро развившегося патологического процесса или обострения хронического патологического процесса в организме, а также на предупреждение, раннюю диагностику и коррекцию возможных нарушений функций поврежденных органов либо систем организма, предупреждение и снижение степени возможной инвалидности, улучшение качества жизни, сохранение работоспособности пациента и его социальную интеграцию в общество. Таким образом, медицинская реабилитация — это целый комплекс терапевтических мероприятий, включающих в себя, как медикаментозные процедуры (базовая лекарственная терапия БП, а также хирургические методы лечения), так и немедикаментозные (в т.ч. лечебная физкультура, физиотерапия, психотерапия, логопедия и мн. др.).
С 1 октября 2018 года вступил в силу приказ Министерства труда и социальной защиты Российской Федерации от 03.09.2018 №572н «Об утверждении профессионального стандарта «Специалист по медицинской реабилитации». Профессиональный стандарт специалиста по медицинской реабилитации определяет его трудовые функции, а также цели, задачи и трудовые характеристики.
Трудовая функция врача физической и реабилитационной медицины, врача по медицинской реабилитации
(в соответствии с приказом Министерства труда и социальной защиты Российской Федерации от 03.09.2018 №572н «Об утверждении профессионального стандарта «Специалист по медицинской реабилитации»)
Трудовые действия
Сбор жалоб, анамнеза жизни и заболевания, социального и профессионального анамнеза у пациентов (их законных представителей), имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Осмотр пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Проведение физикального обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, определение степени выраженности ограничений жизнедеятельности, нарушений функций и структур организма человека в соответствии с Международной классификацией функционирования, ограничений жизнедеятельности и здоровья (далее — МКФ). Выявление отклонений в физическом и психомоторном развитии и (или) состоянии пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Установка предварительного реабилитационного диагноза и составление плана лабораторных обследований и инструментальных исследований пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Направление пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на инструментальное исследование для определения степени выраженности ограничений жизнедеятельности, нарушений функций и структур организма человека. Направление пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на лабораторное обследование для определения степени выраженности ограничений жизнедеятельности, нарушений функций и структур организма человека. Направление пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на консультацию к врачам-специалистам. Направление пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на консультацию к специалистам с высшим профессиональным (немедицинским) образованием, в том числе к логопедам, медицинским психологам, специалистам по физической и бытовой реабилитации, специалистам по социальной работе мультидисциплинарной реабилитационной бригады. Обоснование и постановка реабилитационного диагноза с учетом МКФ с установлением ограничения жизнедеятельности, степени нарушения функций и структур организма человека в соответствии с принятыми критериями и классификациями. Формулирование и обоснование реабилитационного потенциала с учетом МКФ и его корректировка по результатам медицинской реабилитации на различных этапах оказания помощи по медицинской реабилитации. Медицинские показания и противопоказания к назначению технических средств реабилитации и ассистивных технологий пациентам, имеющим нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности.
Разработка плана медицинской реабилитации пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности вне зависимости от возраста, при заболеваниях и (или) состояниях в соответствии с порядком организации медицинской реабилитации, действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи, с учетом стандартов медицинской помощи. Интерпретация данных, полученных при консультировании пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, врачами-специалистами, специалистами с высшим профессиональным (немедицинским) образованием мультидисциплинарной реабилитационной бригады, данных лабораторных, инструментальных и клинических исследований с целью получения представления о степени нарушения различных функций, структур, жизнедеятельности пациента (активности, участия, влияния факторов окружающей среды) Формулирование целей проведения реабилитационных мероприятий на основе реабилитационного диагноза и реабилитационного потенциала на день, на неделю, на весь период пребывания пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, в медицинской организации. Формулирование задач медицинской реабилитации, направленных на достижение целей медицинской реабилитации. Формирование индивидуальной программы медицинской реабилитации, направленной на решение задач и достижение целей медицинской реабилитации с учетом показаний и противопоказаний к использованию отдельных форм и методов медицинской реабилитации. Определение двигательного режима, индивидуальных границ интенсивности применяемых воздействий на пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Определение факторов риска и факторов, ограничивающих проведение мероприятий по реализации индивидуальной программы медицинской реабилитации. Назначение лекарственных препаратов, медицинских изделий и лечебного питания в целях коррекции нарушенных функций и структур организма человека, ограничений жизнедеятельности пациента с различными заболеваниями и (или) состояниями. Оценка эффективности и безопасности применения лекарственных препаратов, медицинских изделий и лечебного питания для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности человека вследствие различных заболеваний и (или) состояний. Назначение физиотерапии в процессе медицинской реабилитации в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи по медицинской реабилитации, с учетом стандартов медицинской помощи. Оценка эффективности и безопасности применения физиотерапии для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Назначение лечебной физкультуры в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи по медицинской реабилитации, с учетом стандартов медицинской помощи. Оценка эффективности и безопасности применения лечебной физкультуры у пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Назначение рефлексотерапии в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи по медицинской реабилитации, с учетом стандартов медицинской помощи. Оценка эффективности и безопасности применения рефлексотерапии для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Определение и подбор технических средств реабилитации (далее — TCP) и ассистивных технологий пациентам с значительными временными (стойкими) нарушениями функций и структур, ограничением жизнедеятельности. Оценка эффективности и безопасности применения TCP и ассистивных технологий для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Определение исполнителей мероприятий по медицинской реабилитации, направленных на решение задач и достижение целей медицинской реабилитации в течение дня, недели, всего периода проведения мероприятий по медицинской реабилитации. Определение двигательного режима, последовательности, интенсивности и длительности выполнения каждого из мероприятий индивидуальной программы медицинской реабилитации. Определение места и формы проведения мероприятий по медицинской реабилитации. Оценка эффективности и безопасности мероприятий индивидуальной программы медицинской реабилитации. Определение критериев достижения целей и решения задач медицинской реабилитации. Организация и проведение мониторинга и мультидисциплинарного обсуждения результатов реализации индивидуальной программы медицинской реабилитации в режиме реального времени в зависимости от тяжести клинического состояния пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Оценка результатов реализации индивидуальной программы медицинской реабилитации. Формулирование рекомендаций по продолжению мероприятий медицинской реабилитации. Профилактика или лечение осложнений, побочных действий, нежелательных реакций, в том числе серьезных и непредвиденных, возникших в результате проведения медицинской реабилитации. Направление пациентов, имеющих стойкое нарушение функции организма человека, на медико-социальную экспертизу; оформление необходимой медицинской документации. Оказание медицинской помощи в неотложной форме пациентам, имеющим нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности.
Необходимые умения
Осуществлять сбор жалоб, анамнеза жизни и заболевания, социального и профессионального анамнеза у пациентов (их законных представителей), имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Проводить осмотры и обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Интерпретировать и анализировать информацию, полученную от пациентов (их законных представителей), имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на основании категорий МКФ. Оценивать анатомо-функциональное состояние органов и систем организма человека пациентов в норме и при развитии заболеваний или патологических состояний. Использовать методы осмотра и обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, в числе которых:
— исследование постуральных функций;
— исследование опорных структур и функций;
— исследование возможности изменять положение тела (позы);
— исследование функции перемещения тела с регистрацией кинематических параметров в трех плоскостях;
— исследование функции ходьбы;
— исследование функции и структуры верхней конечности;
— исследование функции и структуры нижней конечности;
— исследование координаторной функции;
— исследование функции восприятия;
— исследование функции выносливости;
— исследование функций глотания;
— исследование функций метаболизма (метаболометрия, метаболография);
— исследование функции выделения (дневник мочеиспускания и дефекации);
— скрининговое исследование высших психических функций (памяти, внимания, мышления, речи, управляющих функций);
— скрининговое исследование тревоги и депрессии;
— исследование нейрофизиологических параметров в режиме реального времени.
Использовать методы исследования жизнедеятельности пациентов, имеющих нарушения функций и структур организма человека, в числе которых:
— исследование способности к обучению и применению знаний;
— исследование способности к выполнению общих задач и требований;
— исследование способности к коммуникации;
— исследование мобильности в обычных условиях;
— исследование способности к самообслуживанию;
— исследование способности к активности в бытовой жизни;
— исследование возможности выделения главных сфер в жизни;
— исследование способности к самостоятельности в сообществах. Выявлять отклонения в физическом и психомоторном развитии пациентов в различных возрастных группах. Интерпретировать и анализировать результаты осмотра и обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Обосновывать и планировать объем лабораторного обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Интерпретировать и анализировать результаты лабораторного обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Обосновывать необходимость и объем инструментального исследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельностиИнтерпретировать и анализировать результаты инструментального обследования пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Обосновывать необходимость направления на консультации к врачам-специалистам пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Обосновывать необходимость направления на консультацию к специалистам с высшим профессиональным (немедицинским) образованием мультидисциплинарной реабилитационной бригады пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельностиИнтерпретировать и анализировать данные, полученные при консультировании пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, врачами-специалистами. Интерпретировать данные, полученные при консультировании пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, специалистами с высшим профессиональным (немедицинским) образованием (логопеды, медицинские психологи, специалисты по физической и бытовой реабилитации, специалисты по социальной работе) мультидисциплинарной реабилитационной бригады. Выявлять клинические симптомы и синдромы у пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Использовать алгоритм постановки реабилитационного диагноза с учетом МКФ, применять методы дифференциальной диагностики пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Интерпретировать и анализировать результаты осмотра пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Обосновывать и планировать объем дополнительных инструментальных исследований пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Интерпретировать и анализировать результаты дополнительного инструментального исследования пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Обосновывать и планировать объем дополнительного лабораторного обследования пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Интерпретировать и анализировать результаты дополнительного лабораторного обследования пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека, Обосновывать и планировать объем консультирования врачами-специалистами пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Интерпретировать и анализировать результаты консультаций врачей-специалистов пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека, Интерпретировать и анализировать полученные результаты обследования пациента, имеющего ограничения жизнедеятельности, нарушения функций и структур организма человека, при необходимости обосновывать и планировать объем дополнительных исследований. Интерпретировать результаты сбора информации о заболевании, образе жизни, характере и степени нарушения функций и жизнедеятельности пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Обобщать данные, полученные при обследовании, формулировать и обосновывать реабилитационный диагноз с учетом МКФ и составлять план лабораторных, инструментальных и клинических обследований пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Обобщать данные, полученные при обследовании, формулировать и обосновывать реабилитационный потенциал с учетом МКФ и корректировать его в зависимости от результата медицинской реабилитации на различных этапах оказания реабилитационной помощи. Обобщать данные, полученные при обследовании, формулировать и обосновывать реабилитационные цели и задачи с учетом МКФ и корректировать их в зависимости от результата медицинской реабилитации на различных этапах оказания реабилитационной помощи. Определять медицинские показания для назначения технических средств реабилитации и ассистивных технологий пациентам, имеющим ограничения жизнедеятельности, нарушения функций и структур организма человека. Использовать информационно-компьютерные технологии.
Составлять заключение о состоянии нарушенных и сохранных функций и структур пациента, состоянии его жизнедеятельности по данным всестороннего обследования с учетом МКФ. Интерпретировать данные, полученные при консультировании пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, врачами-специалистами, специалистами с высшим профессиональным (немедицинским) образованием (логопедам, медицинским психологам, специалистами по физической и бытовой реабилитации, специалистами по социальной работе) мультидисциплинарной реабилитационной бригады; данные лабораторных, инструментальных и клинических исследований с целью получения представления о степени нарушения различных функций, структур, жизнедеятельности пациента (активности, участия, влияния факторов окружающей среды) вследствие заболевания и (или) состояния. Определять реабилитационный потенциал, формулировать реабилитационный диагноз с учетом МКФ и реабилитационный план. Разрабатывать индивидуальную программу медицинской реабилитации. Формулировать цель проведения реабилитационных мероприятий. Формулировать задачи медицинской реабилитации для каждого специалиста мультидисциплинарной реабилитационной бригады. Обосновывать применение лекарственных препаратов, медицинских изделий, диетического питания, немедикаментозного лечения для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи, с учетом стандартов медицинской помощи. Определять последовательность применения лекарственных препаратов, немедикаментозной терапии для пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи, с учетом стандартов медицинской помощи. Назначать лекарственные препараты, медицинские изделия и лечебное питание в целях коррекции нарушенных функций и структур организма человека, ограниченной жизнедеятельности пациента при заболеваниях и (или) состояниях; проводить мероприятия по вторичной профилактике в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи по медицинской реабилитации, с учетом стандартов медицинской помощи. Проводить мониторинг эффективности и безопасности применения лекарственных препаратов, медицинских изделий и лечебного питания в целях коррекции нарушенных функций и структур организма человека, ограниченной жизнедеятельности пациента при заболеваниях и (или) состояниях. Назначать физиотерапию в целях коррекции нарушенных функций и структур организма, ограниченной жизнедеятельности пациента при заболеваниях и (или) состояниях. Оценивать эффективность и безопасность применения физиотерапии в целях коррекции нарушенных функций и структур организма, ограниченной жизнедеятельности пациента при заболеваниях и (или) состояниях. Определять двигательный режим, индивидуальные границы интенсивности применяемых воздействий в процессе медицинской реабилитации. Назначать средства лечебной физкультуры, роботизированную терапию, экзоскелеты, оборудование с биологической обратной связью и интерфейсами «мозг — компьютер» в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи по медицинской реабилитации, с учетом стандартов медицинской помощи. Оценивать эффективность и безопасность применения средств лечебной физкультуры, роботизированной терапии, экзоскелетов, оборудования с биологической обратной связью и интерфейсами «мозг — компьютер» в целях коррекции нарушенных функций и структур, ограниченной жизнедеятельности пациента. Выбирать ведущих специалистов — исполнителей реабилитационных мероприятий на конкретный период для последовательного решения поставленных задач. Выбирать критерии эффективности и безопасности мероприятий по медицинской реабилитации. Определять факторы риска и ограничивающие факторы проведения мероприятий по реализации индивидуальной программы медицинской реабилитации. Назначать TCP пациентам со значительными временными или стойкими нарушениями функций и структур организма человека, ограничением жизнедеятельности. Направлять для продолжения мероприятий по медицинской реабилитации пациентов в соответствии с реабилитационным потенциалом и реабилитационными целями в медицинские организации соответствующих этапов оказания помощи по медицинской реабилитации (реанимационное отделение, специализированное отделение по профилю оказываемой помощи, специализированное отделение медицинской реабилитации, дневной стационар, отделение медицинской реабилитации поликлиники, санаторно-курортной организации, телемедицинский центр) Определять последовательность, интенсивность и длительность выполнения каждого из мероприятий индивидуальной программы медицинской реабилитации. Определять критерии достижения целей и решения задач медицинской реабилитации. Организовывать и проводить мониторинг и мультидисциплинарное обсуждение результатов реализации индивидуальной программы медицинской реабилитации в режиме реального времени в зависимости от тяжести клинического состояния пациента, имеющего нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Определять показания и формулировать рекомендации по продолжению мероприятий медицинской реабилитации. Проводить профилактику или лечение осложнений, побочных действий, нежелательных реакций, в том числе серьезных и непредвиденных, возникших в результате реабилитационных мероприятий или манипуляций, применения лекарственных препаратов или медицинских изделий, лечебного питания. Направлять пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, на медико-социальную экспертизу. Консультировать родственников, (законных представителей) по вопросам проведения реабилитационных мероприятий, выполнения индивидуальной программы медицинской реабилитации, вторичной и третичной профилактики, ухода. Необходимые знания. Порядок организации медицинской реабилитации. Порядки оказания медицинской помощи пациентам по профилям заболеваний и (или) состояний, в связи с развитием которых проводятся мероприятия по медицинской реабилитации. Стандарты первичной специализированной медико-санитарной помощи, специализированной, в том числе высокотехнологичной, медицинской помощи при заболеваниях и (или) состояниях, в связи с развитием которых проводятся мероприятия по медицинской реабилитации. Клинические рекомендации (протоколы лечения) по вопросам оказания медицинской помощи пациентам с заболеваниями или состояниями, в связи с развитием которых проводятся мероприятия по медицинской реабилитации. Методы медицинской реабилитации пациентов с различными заболеваниями или состояниями. Механизм действия лекарственных препаратов, медицинских изделий и лечебного питания, применяемых при медицинской реабилитации; медицинские показания и медицинские противопоказания к назначению; возможные осложнения, побочные действия, нежелательные реакции, в том числе серьезные и непредвиденные. Методы немедикаментозного лечения, применяемые в медицинской реабилитации; медицинские показания и медицинские противопоказания; возможные осложнения, побочные действия, нежелательные реакции, в том числе серьезные и непредвиденные. Особенности нарушения функций, активности и участия при основных заболеваниях, являющихся причиной инвалидности, неинфекционных заболеваниях, проблемах перинатального периода. Патогенез и саногенез основных заболеваний, являющихся причиной инвалидности, неинфекционных заболеваний, патологических состояний перинатального периода. Физическое развитие ребенка первых трех лет жизни. Онтогенез функциональной системы движения первых трех лет жизни. Развитие когнитивных функций у ребенка первых трех лет жизни. Развитие речевых функций у ребенка первых трех лет жизни. Методы оценки, классификация вариантов нарушений двигательных функций, высших психических функций, психоэмоционального состояния, речи, письма, гигиенических навыков, бытовых навыков и других аспектов функционирования организма человека. Функциональные классы в оценке степени нарушения функций по рекомендации Всемирной организации здравоохранения, градации функциональных классов. Общие основы медицинской реабилитации, цели и задачи проведения реабилитационных мероприятий на различных этапах медицинской реабилитации. Теория адаптации, дезадаптации и стресса. Механизм воздействия реабилитационных мероприятий на организм пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельностиРеабилитационный потенциал, методы определения реабилитационного потенциала, факторы реабилитационного потенциала, использование реабилитационного потенциала. Основы паллиативной помощи. Двигательные режимы, индивидуальные границы интенсивности применяемых воздействий в процессе медицинской реабилитации. Методика разработки индивидуальных программ медицинской реабилитации в целях профилактики отклонений в физическом развитии с учетом возраста, влияние заболевания на физическое и психомоторное развитие и функциональный статус человека. Методика разработки комплекса методов медицинской реабилитации для самостоятельного применения с учетом возраста, заболевания и функционального статуса. Индивидуальная программа медицинской реабилитации в процессе медицинской реабилитации, индивидуальная программа реабилитации пациента со стойкими нарушениями функций и структур организма человека, ограничения жизнедеятельности при заболеваниях и (или) состояниях; принципы назначения, преемственность мероприятий по медицинской реабилитации. Принципы определения преимуществ применения того или иного средства, метода (в том числе медикаментозных средств, кинезотерапии, механотерапии, физиотерапии, робототехники, экзоскелетов, информационных технологий, логотерапии, психологической коррекции, эрготерапии, TCP) или формы (индивидуальное, групповое занятие, занятие с применением телемедицинских технологий) медицинской реабилитации на различных этапах ее проведения, в различные периоды течения заболеваний и (или) состояний, при устойчивых нарушениях функций и структур организма человека, ограничении жизнедеятельности. Критерии завершения реабилитационных мероприятий и принципы маршрутизации пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, для оказания помощи по медицинской реабилитации на последующих этапах или ее завершения. Принципы мультидисциплинарной работы в медицинской реабилитации, управление процессом медицинской реабилитации. Система медицинской и социальной реабилитации в Российской Федерации. Медико-социальная экспертиза нетрудоспособности в Российской Федерации TCP: классификация, правила назначения. Основы применения логопедической коррекции. Основы применения социально-бытовой адаптации. Основы применения TCP. Медицинские показания и противопоказания сочетания различных средств, форм и методов медицинской реабилитации пациентов различного профиля, при различном клиническом состоянии пациента. Факторы риска при проведении реабилитационных мероприятий; факторы, задерживающие восстановление; факторы, препятствующие восстановлению нарушенных функций и структур, ограничивающих жизнедеятельность пациента. Принципы медицинской реабилитации в различные периоды течения заболеваний и (или) состояний: предоперационный, послеоперационный, острейший, острый, подострый, ранний восстановительный, поздний восстановительный. Этапы и принципы восстановления нарушенных функций и структур, ограниченных активности и участия; влияние на пациентов факторов окружающей среды при основных заболеваниях, являющихся причиной инвалидности, неинфекционных заболеваниях и (или) состояниях, проблемах перинатального периода. Принципы потенцирования, кумуляции и угасания эффекта от используемых вмешательств, принципы безопасности проведения различных вмешательств или стимуляций в процессе медицинской реабилитации. Теория адаптации, теория функциональных систем, теория о типовых патологических процессах, утомление, переутомление, перенапряжение. Универсальные и специальные критерии качества оказания помощи по медицинской реабилитации. Способы предотвращения или устранения осложнений, побочных действий, нежелательных реакций, в том числе серьезных и непредвиденных, возникших при обследовании или лечении пациентов, имеющих нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности. Принципы и методы оказания неотложной медицинской помощи пациентам, имеющим нарушения функций и структур организма человека и последовавшие за ними ограничения жизнедеятельности, в том числе в соответствии с действующими порядками оказания медицинской помощи, клиническими рекомендациями (протоколами лечения) по вопросам оказания медицинской помощи, с учетом стандартов медицинской помощи.
Необходимые знания
Основные клинические проявления заболеваний и (или) состояний нервной, иммунной, сердечно-сосудистой, дыхательной, пищеварительной, мочеполовой систем и системы крови, приводящие к тяжелым осложнениям и (или) угрожающим жизни, определение тактики ведения пациента с целью их предотвращения. Порядок организации медицинской реабилитации. Клинические рекомендации (протоколы лечения) по вопросам оказания медицинской помощи, стандарты первичной специализированной медико-санитарной помощи, специализированной, в том числе высокотехнологичной, медицинской помощи при заболеваниях и (или) состояниях по вопросам проведения медицинской реабилитации. Общие вопросы организации оказания медицинской помощи населению. Порядки оказания медицинской помощи, клинические рекомендации (протоколы лечения) по вопросам оказания медицинской помощи по медицинской реабилитации. Стандарты первичной специализированной медико-санитарной помощи, специализированной, в том числе высокотехнологичной, медицинской помощи при заболеваниях и (или) состояниях, в связи с развитием которых проводятся мероприятия по медицинской реабилитации. Методика сбора анамнеза жизни и жалоб у пациентов (их законных представителей), имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Методика осмотра и обследования пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Закономерности развития и функционирования здорового организма человека в различные возрастные периоды и механизмы обеспечения здоровья с позиции теории функциональных систем; особенности регуляции функциональных систем организма человека в норме и при развитии патологических процессов. Особенности взаимодействия пациента, имеющего ограничения жизнедеятельности, нарушения функций и структур организма человека, с субъектами и объектами окружающей среды в норме и при развитии различных заболеваний или состояний. Этиология, патогенез, клиническая картина нарушений функции, структур организма человека, жизнедеятельности, дифференциальная диагностика, особенности течения восстановительного периода, осложнения и возможные исходы реабилитационного процесса при заболеваниях и (или) состояниях. Клиническая картина, особенности течения осложнений основного и сопутствующих заболеваний у пациентов с основными заболеваниями, являющимися причиной развития инвалидности. Симптомы и синдромы осложнений, побочных действий, нежелательных реакций, в том числе серьезных и непредвиденных, возникших в результате диагностических и реабилитационных процедур у пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека, при различных заболеваниях и (или) состояниях. Современные методы клинической и параклинической диагностики нарушений функций, структур организма человека и жизнедеятельности. Медицинские показания и медицинские противопоказания к использованию методов инструментальной диагностики пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Медицинские показания к использованию методов лабораторной диагностики пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Классы и категории нарушений функций, структур организма человека нарушения функций и структур организма человека. Классы и категории нарушений функций, структур организма человека и ограничения жизнедеятельности. Методики проведения и алгоритм выбора специальных функциональных проб, тестов и шкал для пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Методика формулирования реабилитационного диагноза и реабилитационного потенциала. Методики анализа потребности в назначении технических средств реабилитации и ассистивных технологий для пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Методики анализа окружающей среды (дома, в квартире, на рабочем месте, в медицинской организации) пациентов, имеющих ограничения жизнедеятельности, нарушения функций и структур организма человека. Международная классификация болезней. Медицинские показания к направлению пациента, имеющего ограничения жизнедеятельности, нарушения функций и структур организма человека, к врачам-специалистам. Медицинские показания для оказания пациентам, имеющим ограничения жизнедеятельности, нарушения функций и структур организма человека, медицинской помощи в неотложной форме.
Цель и задачи реабилитации при болезни Паркинсона
Целью реабилитации при БП является улучшение качества жизни путем поддержания независимости пациента, его безопасности и благополучия, а также улучшения его двигательных функций и уменьшения степени выраженности неврологического дефицита. Это достигается за счет профилактики малоподвижного образа жизни и падений, улучшения повседневной активности и снижение ограничений в повседневной деятельности.
К общим принципам реабилитации пациентов с БП относят:
1. раннее начало и преемственность на всех этапах;
2. мультидисциплинарный и персонифицированный подход;
3. постановка индивидуальных задач — реабилитационных целей (долгосрочных и краткосрочных), согласованных с пациентом и его родственниками;
4. активное участие пациентов в программе реабилитации;
5. комплексность применяемых методов;
6. регулярность и адекватная интенсивность занятий, постепенное увеличение сложности и скорости выполнения упражнений с учетом и подкреплением достигаемых успехов.
Основными долгосрочными задачами реабилитации у пациентов с БП являются:
1. обеспечение безопасности и независимости пациента в повседневной жизни с акцентом на трансфер, постуральную устойчивость, мышечную силу, объем движений и ходьбу;
2. сохранение или улучшение двигательной активности;
3. сохранение и увеличение выносливости;
4. профилактика падений;
5. профилактика пролежней;
6. улучшение когнитивных расстройств
7. улучшение эмоциональных расстройств
8. понимание ограничения в повседневной жизни в связи с нарушенными двигательными функциями.
Для правильного построения процесса медицинской реабилитации и соблюдения основных ее принципов важно четкое и однозначное понимание основных терминов, применяемых в отношении медицинской реабилитации.
Термин «междисциплинарное взаимодействие» уже давно используется в клинической медицине на разных уровнях оказания медицинской помощи и, как правило, применяется в отношении инсультной категории пациентов в процессе проведения лечебно-диагностических и реабилитационных мероприятий. Однако полноценного понимания, что же под собой подразумевает меж- или мультидисциплинарное взаимодействие, в чем его особенности, принципы и преимущества, как определенной реабилитационной технологии, пока нет у большинства клиницистов-реабилитологов.
В приказе Министерства здравоохранения Российской Федерации «О порядке организации медицинской помощи по медицинской реабилитации» от 29 декабря 2012 г. дается следующее определение: «Мультидисциплинарный подход к осуществлению реабилитационных мероприятий — применение комплекса мер медицинского, педагогического, профессионального и социального характера при взаимодействии специалистов различного профиля, включая различные виды помощи по преодолению последствий заболевания, изменению образа жизни, снижению воздействия факторов риска с целью определения цели реабилитации, необходимости и достаточности, продолжительности, последовательности и эффективности участия каждого специалиста в каждый конкретный момент времени течения реабилитационного процесса». Мультидисциплинарный подход осуществляется членами мультидисциплинарной бригады, включающей:
— врачей-специалистов по профилю оказываемой медицинской помощи; врача-терапевта участкового, врача-педиатра участкового;
— врача по медицинской реабилитации;
— врача по лечебной физкультуре и спортивной медицине, врача-физиотерапевта, медицинского психолога;
— по показаниям — врача-рефлексотерапевта, врача мануальной терапии, отделений (кабинетов) реабилитации медицинской организации, отделения (кабинета) физиотерапии, отделения (кабинета) лечебной физкультуры, кабинетов рефлексотерапии, мануальной терапии медицинской организации по заявке врача реаниматолога, врача отделения интенсивной терапии, лечащего врача, врача-специалиста;
— медицинских палатных сестер отделения реанимации и интенсивной терапии, медицинских сестер палатных профильных отделений;
— по показаниям — специалистов, имеющих высшее немедицинское образование в соответствии с требованиями организации деятельности по специальности: по коррекционной педагогике (логопедии), нейропсихологов, инструкторов-методистов по лечебной физкультуре; специалистов по социальной работе;
— по показаниям — врачей функциональной, ультразвуковой, лучевой диагностики, специалистов клинической лабораторной диагностики и др. специалистов, осуществляющих контроль безопасности и эффективности проведения реабилитационных мероприятий в соответствии с порядками оказания специализированной медицинской помощи, настоящим порядком, а также порядками оказания медицинской помощи по лечебной физкультуре, физиотерапии, мануальной терапии, клинической психологии и рефлексотерапии.
Реабилитационная мультидисциплинарная бригада определяет индивидуальную программу реабилитации пациента, осуществляет текущее медицинское наблюдение и проведение комплекса реабилитационных мероприятий.
Междисциплинарное взаимодействие уже давно доказало на практике свою высокую эффективность в достижении целей медицинской реабилитации в наиболее короткие сроки за счет снижения количества осложнений, связанных с основным заболеванием, четкого контроля специалистами разного профиля безопасности и эффективности мероприятий по медицинской реабилитации и возможности построения процесса медицинской реабилитации пошагово и комплексно. Особенно важное значение имеет организация работы междисциплинарной бригады на I этапе медицинской реабилитации, когда четкое взаимодействие специалистов разного профиля обеспечивает наиболее быстрые темпы адаптации пациента к физическим нагрузкам, способствует расширению его двигательного режима и снижает до минимума риск развития осложнений, связанных с гиподинамией и клиническими особенностями течения основного заболевания.
Ключевым моментом комплексного построения реабилитационной программы является определение реабилитационного диагноза. Реабилитационный диагноз — диагноз, отражающий критерии оценки функциональных последствий заболевания (травмы), включающий в себя описание возникшего повреждения и последовавших за этим нарушений бытовых и профессиональных навыков; ограничения активности и участия в значимых для индивида событиях частной и общественной жизни; влияния факторов окружающей среды, облегчающих или осложняющих выполнение основных функций. Реабилитационный диагноз должен включать как клинико-функциональный диагноз, отражающий характер и выраженность анатомо-физиологических и функциональных нарушений, так и характеристику нарушений привычной жизнедеятельности. Реабилитационный диагноз устанавливается на основании глубинного реабилитационного обследования пациента, выявления функционального дефицита, оценки компенсаторных возможностей организма, степени приспособленности к социально-бытовой среде, владения трудовыми и бытовыми навыками. Постановка реабилитационного диагноза — одна из важнейших задач, которая ставится перед междисциплинарной бригадой. В процессе формулировки реабилитационного диагноза рекомендовано использовать Международную классификацию функционирования (МКФ). Как классификация, МКФ системно группирует различные домены индивида с определенным изменением здоровья (например, указывает, что индивид с заболеванием или расстройством делает или способен делать). Функционирование является общим термином для констатации положительного или нейтрального аспектов функций организма, активности и участия, точно так же термин ограничения жизнедеятельности относится ко всем нарушениям, ограничениям активности и ограничениям возможности участия. Кроме того, МКФ содержит перечень факторов окружающей среды, которые взаимодействуют со всеми этими категориями. Таким образом, она позволяет пользователю практически отразить профиль функционирования и ограничений жизнедеятельности индивида, отраженный в рамках различных доменов. МКФ принадлежит к «семье» международных классификаций, разработанных Всемирной Организацией Здравоохранения (ВОЗ), которые применимы к различным аспектам здоровья. «Семья» международных классификаций ВОЗ обеспечивает общие правила кодирования широкого круга информации, связанной со здоровьем (например, диагноз, функционирование и ограничение жизнедеятельности, основание для обращения за медицинской помощью), и использует стандартизованный общий язык, позволяющий общаться по проблемам, связанным со здоровьем и здравоохранением, во всем мире в различных дисциплинах и отраслях науки. МКФ — это многоцелевая классификация, разработанная для использования в различных дисциплинах и областях. Ее специфические цели могут быть определены как следующие: обеспечить научную основу для понимания и изучения показателей здоровья и показателей, связанных со здоровьем, результатов вмешательств и определяющих их факторов; сформировать общий язык для описания показателей здоровья и показателей, связанных со здоровьем, с целью улучшения взаимопонимания между различными пользователями: работниками здравоохранения, исследователями, администраторами и обществом, включая людей с ограничениями жизнедеятельности; сделать сравнимой информацию в разных странах, сферах здравоохранения, службах и во времени; обеспечить систематизированную схему кодирования для информационных систем здоровья. МКФ в руках специалистов-реабилитологов — это, прежде всего унифицированный всеобъемлющий инструмент для постановки реабилитационного диагноза. Четко определенный и грамотно сформулированный (на основе принципов и позиций-доменов МКФ) реабилитационный диагноз — залог правильно построенной реабилитационной программы.
Пациенты с БП сталкиваются с большим разнообразием нарушений, прежде всего первично или вторично связанных с заболеванием, или связанных c побочными действиями противопаркинсонической терапии. Эти нарушения функций, а также активность и участие, и факторы среды, участвующие в обеспечении функционирования отражаются в МКФ. Cписок доменов МКФ, для оценки основных моторных и немоторных функций, активности и участия может быть использован для осмотра и описания пациента с БП. МКФ в реабилитации пациентов с БП необходима для постановки реабилитационного диагноза, определения плана мероприятий реабилитации с оценкой ее эффективности.
Европейские рекомендации по двигательной реабилитации больных с БП (European Physiotherapy Guideline for Parkinson’s disease, 2014) и рекомендации ВОЗ по реабилитации предложили определять продолжительность занятий пациентов с БП в зависимости от их возраста и выбора метода:
У лиц от 18 до 64 лет:
1. Аэробные нагрузки:
— Не менее 150 мин в неделю при средней интенсивности;
— Не менее 75 мин в неделю при высокой интенсивности.
2. Аэробные нагрузки должны выполняться продолжительностью не менее 10 минут.
3. Упражнения на растяжения крупных групп мышц:
— Не мене 2 раз в неделю.
4. Дополнительно можно рекомендовать:
— 300 минут интенсивной аэробной физической активности в неделю;
— или 150 минут интенсивной аэробной физической активности в неделю.
У лиц старше 65 лет используется тот же подход, но при снижении мобильности выполнение упражнений на баланс и профилактику падений осуществляется не менее 3-х раз в неделю.
В периоде «включения» — аэробные нагрузки высокой интенсивности рекомендуется не проводить продолжительностью более 10 минут.
В периоде «выключения» — реабилитация показана, но с ограничениями в методиках. Кроме того, необходимо избегать двойной постановки задач при занятиях. Большинство пациентов с БП не в состоянии выполнять несколько задач одновременно. Двойные задачи могут оказать негативное влияние на ходьбу и баланс, что может привести к небезопасной ситуации в повседневной жизни, а также во время занятий. Избегание выполнения двойной задачи не только во время занятий, а также в повседневной жизни (при ходьбе), повышает безопасность пациентов и может уменьшить риск падения. На поздних стадиях БП необходимо обучать ухаживающих лиц за пациентами реабилитационным методикам, включающим компенсаторные стратегии, трансфер и когнитивный тренинг.
Условно немедикаментозные реабилитационные методы при БП можно разделить на:
1) комплекс различных методик для восстановления и поддержания различных двигательных функций (двигательная реабилитация) в т.ч. классическая лечебная гимнастика, механотерапия, степ-гимнастика, фитбол-гимнастика, танцевально-двигательная терапия, кинезиологическое тейпирование и др.;
2) технологии с БОС и виртуальной реальностью;
3) когнитивный тренинг для улучшения когнитивных функций;
4) социальную поддержку и психотерапию;
5) эрготерапию для поддержания и восстановления повседневных навыков;
6) логопедическую коррекцию.
Главными задачами применения физических упражнений являются улучшение показателей ходьбы (длины шага, скорости ходьбы), улучшение амплитуды движений, физических возможностей (силы, подвижности и выносливости) и равновесия. При этом чаще используется комплекс упражнений, включающий в себя активные или пассивные движения для конечностей и позвоночника, растяжку, силовые упражнения и ходьбу.
В последнее десятилетие по результатам представленных рандомизированных и нерандомизированных исследований была доказана эффективность комплекса физических упражнений, тренинга равновесия и ходьбы на увеличение мобильности и повседневной активности при БП.
Силовые упражнения и упражнения на растяжение. Снижение физической выносливости и развитие мышечной слабости у больных БП с течением заболевания вносят свой вклад в скоростные показатели ходьбы и устойчивости, приводя к высоким рискам падений. По результатам исследований силовые физические упражнения позволяют увеличить мышечную силу и выносливость и улучшить показатели ходьбы и устойчивости. Кроме того, у больных с БП развитие флексорной позы приводит к уменьшению амплитуды движений в туловище и шее, которые являются точками приложения для упражнений на растяжение.
Упражнения на равновесие. Нарушения равновесия появляются на развернутой стадии заболевания и является доминирующей на поздней стадии, приводя к падениям. Применение врачебно-физкультурных комплексов упражнений на равновесие позволяет уменьшить число падений, улучшить контроль над равновесием, уменьшить застывания при ходьбе. Сочетание силовых упражнений и упражнений на равновесие более эффективны для уменьшения постуральной неустойчивости по сравнению с применением только упражнений для коррекции равновесия, что свидетельствует в пользу эффективности комбинированного применения реабилитационных методик. В последнее время для коррекции равновесия при БП была продемонстрирована эффективность сочетания комплекса физических упражнений и баланс-тренинга с помощью стабилометрических платформ (рис. 18).
Аэробный тренинг. Аэробный тренинг — это вид физической нагрузки, при которой мышечные движения совершаются за счет энергии, полученной в ходе аэробного гликолиза, то есть окисления глюкозы кислородом. Типичные аэробные тренировки включают бег, ходьбу, велосипед, активные игры. Аэробные тренировки отличаются длительной продолжительностью (постоянная мышечная работа продолжается более 5 минут), при этом упражнения имеют динамический повторяющийся характер. Аэробный тренинг у больных с БП проводится на беговой дорожке, велотренажере и эллиптическом тренажере (рис. 19). По данным исследований, аэробные тренировки помимо повышения толерантности к физической нагрузке у больных, увеличивают скорость ходьбы, высоту и длину шага вне зависимости от нагрузки, увеличивая в том числе повседневную активность.

Танцевально-двигательная гимнастика. Обращает на себя внимание привлечение танц-терапии, как метода повышения двигательной активности у больных БП. Танцевальные шаги позволяют естественно сочетать разнообразные движения, пространственное восприятие, равновесие, силу, гибкость и физическую активность (как вид аэробных упражнений). В сравнении с традиционными упражнениями доказано достоверное улучшение равновесия, ходьбы и физической выносливости при танц-терапии.
Тренинг ходьбы. Нарушения ходьбы проявляются в виде расстройств инициации ходьбы, уменьшения скорости ходьбы, длины и высоты шага. При попытке идти быстрее у пациентов пропорционально больше увеличивается частота шага, нежели его длина. На ранних стадиях нарушения ходьбы не вызывают серьезных проблем у больных. Но по мере прогрессирования БП нарушения ходьбы становятся более сложными, дополнительное влияние оказывает ахейрокинез, позные нарушения (флексорная поза), постуральная неустойчивость, феномен застывания. Появление феномена застывания при ходьбе часто приводит к падениям. Застывания чаще всего возникают в момент переключения с одной программы движения на другую (при повороте, преодолении порога, прохождении через дверь или узкий проем, ходьбе по неровной поверхности). Пациенты часто прибегают к различным компенсаторным приемам, чтобы преодолеть застывание: используют речевые команды («левой, правой, левой, правой»), зрительные ориентиры (конец трости, трещины в полу, и т.д.), музыкальное сопровождение или метроном, меняют центр тяжести при ходьбе, покачиваются при движении. Ходьба у пациентов БП требует внимания, т.к. при выполнении параллельно другой задачи во время ходьбы (например, общение по телефону во время ходьбы), показатели ходьбы могут ухудшиться и это может привести к падению.
Коррекция ходьбы подразумевает реабилитацию, направленную на увеличение длины и высоты шага, скоростных показателей, коррекцию инициации ходьбы, застываний и профилактику падений. При этом используются аэробные упражнения, тренировка на беговой дорожке или эллиптическом тренажере или велотренажере, танц-терапия, ходьба со зрительными или слуховыми ориентирами, скандинавская ходьба, сенсорная дорожка. Методы профилактики падений включают в себя ходунки, специальные приспособления в доме, специальная обувь, коррекция осанки с помощью специальных приспособлений.
Известная под названием «скандинавская ходьба», северная ходьба, финская ходьба с палками, Nordic Walking — практика прогулок на свежем воздухе с парой модифицированных лыжных палок — появилась по одной из версий около 1940 года в Финляндии благодаря профессиональным лыжникам, стремящимся поддерживать себя в форме вне лыжного сезона. Данная техника ходьбы позволяет включить в работу около 90% всех мышц тела. Ebersbach D.G. предложил «скандинавскую ходьбу» в качестве эффективной тренировки при БП. С 2006 г. при БП стала применяться техника ходьбы с палками, называемая Скандинавской ходьбой. Скандинавская ходьба представляет собой ритмичную ходьбу со специальными палками по определенной методике, напоминающей по своему двигательному рисунку ходьбу на лыжах. Она позволяет улучшить координацию и равновесие; может уменьшить застывания, а значит, обеспечивает большую безопасность движений при ходьбе; поддерживает тонус мышц одновременно верхней и нижней частей тела; уменьшает при ходьбе давление на колени и суставы. «Скандинавская ходьба» также может применяться в качестве аэробных упражнений; идеальна для коррекции осанки, что важно при флексорной позе пациентов с БП; палки помогают двигаться в более быстром темпе. Проведенные исследования продемонстрировали влияние данного вида тренинга на скорость ходьбы и длину шага, а также на увеличение повседневной активности и улучшение качества жизни. Скандинавская ходьбы самый простой и эффективный метод коррекции ходьбы, который можно осуществлять в домашних условиях. Кроме того, результаты наблюдений показали длительную эффективность данной методики. Скандинавская ходьба по сравнению с методикой обучения простой ходьбы позволяет улучшать функциональные параметры ходьбы (способность произвольно менять темп ходьбы и параметры шага, улучшать инициацию при ходьбе).
Применение внешних зрительных или слуховых ориентиров позволяет улучшить показатели ходьбы у больных с БП за счет коркового контроля над движениями. Вероятно, слуховые ориентиры (ритмичные слуховые команды) определяют внешний ритм, который позволяет компенсировать дисфункцию базальных ганглиев, или (в случае зрительных ориентиров) создает зрительное направление ходьбы, который активирует мозжечковый и зрительно-двигательный контроль. Однако, применение внешних ориентиров не всегда позволяет улучшить ходьбу. У слуховых ориентиров выделяют непрерывные сигналы с заданным ритмом и «однократные». Сигналы с заданным ритмом определяют и контролируют темп ходьбы. При этом для начала нужно подбирать ритм с помощью тестирования, например с помощью теста 10-метровой ходьбы. Однократные сигналы могут применяться для концентрации внимания при поддержании равновесия, а также при выполнении движений (например, инициация ходьбы после застывания, или при вставании со стула). Для слуховых сигналов может можно использовать плеер с ритмичной музыкой, метроном или подсчет вслух (больным или ухаживающим лицом), зрительных сигналов — полосы на полу, применение трости при ходьбе, фокусирование внимания на каком-либо предмете, тактильных сигналов — нажатие на бедро или стопу, когнитивных сигналов — представить мысленный образ нужной длины шага.
Технологии с БОС и виртуальной реальностью. Еще одним из самых современных методов реабилитации являются технологии виртуальной реальности с биологической обратной связью, имеющий сложный компьютерный интерфейс, осуществляющий симуляцию в реальном времени и интерактивное взаимодействие с мультимодальными сенсорными раздражителями. При тренинге используются зрительные, слуховые и тактильные стимулы. С помощью виртуальной реальности можно в игровой форме проводить комбинированный тренинг за счет усиления произвольного контроля за движениями и выполнения сложных когнитивных задач на внимание, планирование действий, переключение с одной задачи на другую. Результаты рандомизированных клинических исследований по влиянию виртуальной реальности на выраженность нарушений ходьбы и устойчивости при БП свидетельствуют о достаточной эффективности данного метода. Большинство авторов отмечают, что эффект от курса реабилитации с помощью технологий виртуальной реальности сохраняется дольше, чем при других методах реабилитации.
Новейшей реабилитационной методикой является реабилитация с использованием мультисенсорной виртуальной среды (рис. 20). Это реабилитационная интерактивная безмаркерная система виртуальной реальности для коррекции двигательных и когнитивных нарушений. Она основана на оптико-электронной инфракрасной безмаркерной технологии распознавания движений, создает виртуальные изображения на горизонтальных и вертикальных поверхностях с дополнительной звуковой и обонятельной средой. При данном виде тренинга возможно сочетание аэробного тренинга с сложной системой афферентной стимуляции и влияние на эмоциональный фон пациента, а также использование программ когнитивного обучающего тренинга.

Когнитивная реабилитация. Помимо двигательных расстройств, существенным инвалидизирующим фактором, нарушающим социальную адаптацию больных с БП, являются выраженные когнитивные нарушения. В связи с тем, что основными доказанными предикторами выраженных когнитивных нарушений являются возраст, быстрый темп прогрессирования заболевания, длительность заболевания, тяжесть двигательных нарушений с преобладанием аксиальных симптомов, рациональным является сочетание двигательной реабилитации и нейропсихологическим тренингом. При БП характерно преобладание нейродинамических и регуляторных когнитивных расстройств, отражающее избирательное вовлечение подкорково-лобных систем. Основным методом нейропсихологической реабилитации является восстановительное обучение. В его задачи входит компенсация когнитивного дефицита путем перестройки функциональных когнитивных систем, обучение пациентов применению эффективных когнитивных стратегий, улучшение эмоционального состояния и повышение самооценку пациентов.
Когнитивная реабилитация у больных БП направлен на тренинг памяти (зрительной, слухоречевой), психомоторных функций (времени реакции), зрительно-пространственных функций, вербальной активности и регуляторных функций. Существуют различные методики когнитивного тренинга. В течение последних лет когнитивный тренинг стал проводиться с помощью специальных разработанных компьтеризированных программ с биологической обратной связью. Опубликованные результаты рандомизированных клинических исследований свидетельствуют о достоверном улучшении когнитивных функций, прежде всего регуляторных, нейродинамики и психомоторных реакций на фоне когнитивного тренинга. Для определения программы когнитивного тренинга необходим индивидуальный подход с предварительным нейропсихологическимисследованием для определения структуры и выраженности когнитивных нарушений.
В настоящее время наибольший интерес представляет применение компьютеризированных программ когнитивной реабилитации, систем биоуправления с обратной связью, тренажеров с мультисенсорной виртуальной средой.
С помощью компьютеризированных программ когнитивной реабилитации может проводится одновременный тренинг зрительно-пространственных функций, внимания, и регуляторных функций с переключением когнитивных программ (с визуомоторной на аудиомоторную). На базе многофункциональной платформы для биомеханической диагностики возможно проводить тренировки одновременно направленные как на улучшение двигательных функций, так и когнитивный тренинг.
Медикаментозная терапия
В лечении БП можно выделить три основных направления:
1) нейпротекторную терапию, целью которой является замедлить или остановить дегенерацию нейронов головного мозга;
2) симптоматическую терапию, позволяющую уменьшить основные симптомы заболевания за счет коррекции возникающего в мозге нейрохимического и нейрофизиологического дисбаланса;
3) физическую и социально-психологическую реабилитацию.
К числу нейропротекторных относятся 3 группы методов: 1) методы, предупреждающие развитие нейродегенеративных изменений в клетке; 2) методы, обеспечивающие функциональное восстановление частично поврежденных, но жизнеспособных клеток; 3) методы, обеспечивающие увеличение числа нейронов, например, путем импланатации новых клеток или стимулирования деления существующих клеток.
В последние годы экспериментальные и клинические испытания прошли несколько десятков средств, потенциально способных влиять на различные стадии нейродегенеративного каскада, в конечном итоге ведущего к гибели клеток: окислительный стресс, митохондриальная дисфункция, токсическое действие глутамата, нарушения гомеостаза кальция, воспаление, агрегация белков, апоптоз (антиоксиданы, антагонисты глутамата, блокаторы кальциевых каналов, противовоспалительные средства, трофические факторы и т.д.), однако пока их эффективность доказать не удалось.
В настоящее время к числу противопаркинсонических средств (таб. 9), применяемых при БП, относят 6 групп лекарственных средств:
— препараты, содержащие леводопу;
— агонисты дофаминовых рецепторов;
— холинолитики (антихолинергические средства);
— препараты амантадина;
— ингибиторы моноаминооксидазы типа В;
— ингибиторы катехол-О-метилтрансферазы.
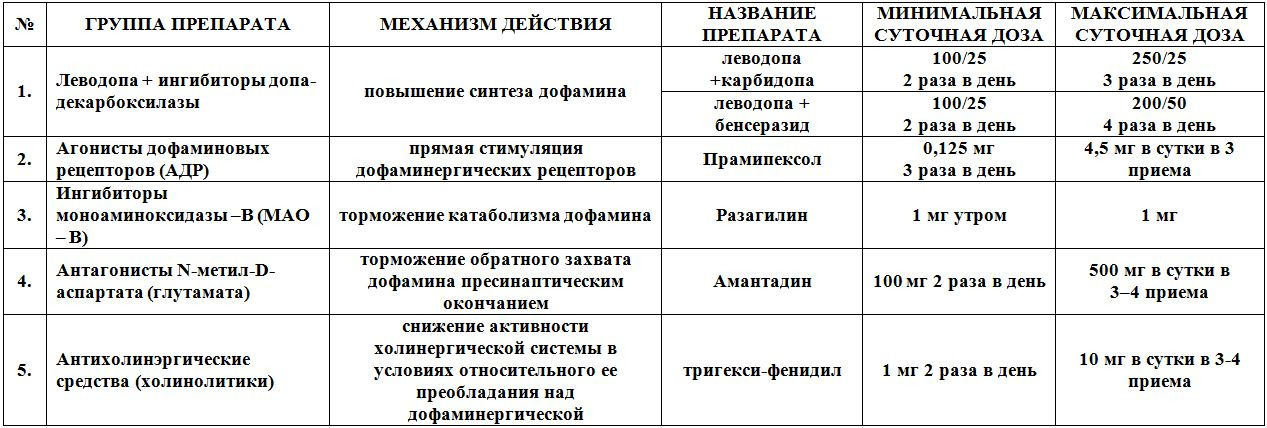
Дисбаланс при БП характеризуется снижением уровня дофамина в связи с дегенерацией нигростриарных нейронов и относительным (или абсолютным) повышением активности холинергических и глутаматергических систем. Фармакотерапию, направленную на коррекцию нейротрансмиттерного дисбаланса, можно с определенной точки зрения считать не только симптоматической, но и патогенетической терапией.
Для коррекции относительного или абсолютного повышения холинергической активности применяются холинолитики, для снижения активности глутаматергической системы — препараты амантадина, для повышения дофаминергической активности применяются препараты леводопы, ингибиторы моноаминооксидазы типа В, ингибиторы катехол-О-метилтрансферазы, агонисты дофаминовых рецепторов. Поскольку механизм действия препаратов этих групп различен, их при необходимости можно сочетать в рамках комбинированной терапии.
Тактика ведения пациентов с БП зависит от ряда факторов, в том числе от выраженности функциональной недостаточности, формы заболевания, возраста больного, индивидуальной чувствительности к препаратам, фармакоэкономических соображений.
Задачей терапии, прежде всего является восстановление нарушенных двигательных функций при использовании минимальных эффективных доз препаратов. В течение первых месяцев болезни, когда проявления заболевания минимальны и не нарушают повседневной социальной или бытовой активности, лекарственная терапия может не назначаться. В начале лечения обычно прибегают к монотерапии, а в случае снижения ее эффективности при прогрессировании заболевания переходят к комбинированной терапии.
Препараты леводопы.
Появление препаратов леводопы в 1960-70-х годах позволило на годы отсрочить момент наступления инвалидизации и развития летального исхода у пациентов с БП. В настоящее время препараты леводопы остаются наиболее эффективными противопаркинсоническими средствами и «золотым стандартом» лечения. Леводопа (L-ДОФА) является непосредственным метаболическим предшественником дофамина, но, в отличие от него, может переноситься через гематоэнцефалический барьер с помощью специальной транспорной системы. Она захватывается окончаниями сохранившихся дофаминергических нигростриарных нейронов и, подвергаясь в них декарбоксилированию, превращается в дофамин, который выделяется в синаптическую щель, поддерживая адекватное функциональное состояние нейронов полосатого тела.
После приема внутрь леводопа почти полностью всасывается в тонком кишечнике, транспортируясь через стенку кишечника специальным переносчиком. Однако 70% дозы метаболизируется в печени, почках и крови под действием периферической ДОФА-декарбоксилазы, и лишь 1% принятой дозы достигает головного мозга. поэтому современные препараты содержат комбинацию леводопы с ингибиторами декарбоксилазы –карбидопой или бензеразидом, которые не пересекают гематоэнцефалический барьер и тормозят превращение леводопы в дофамин на периферии. Это позволяет уменьшить дозу и вероятность периферических побочных эффектов (ортостатическая гипотензия, тошнота).
Препараты леводопы эффективны в отношении всех основных симптомов заболевания — гипокинезии, тремора, ригидности. Терапевтическое действие наступает у 95% больных болезнью Паркинсона. Однако леводопа не предупреждает прогрессирования заболевания, мало влияет на выраженность так называемых аксиальных симптомов (дизартрия, дисфагия, постуральная неустойчивость), а также психические и вегетативные нарушения, которые на фоне лечения продолжают нарастать.
Побочные эффекты леводопы подразделяют на периферические (тошнота, рвота, тахикардия, приступы гипергидроза, ортостатическая гипотензия) и центральные (галлюцинации и другие психические изменения, затрудненное засыпания или сонливость, дискинезии).
В течение нескольких лет леводопа у подавляющего большинства больных БП способна обеспечить адекватный уровень двигательной активности. Несмотря на короткий период полужизни леводопы в крови (60—90 мин), ее эффект в первые годы лечения при 3-х кратном приеме остается стабильным в течение суток (так называемый период «медового месяца»). Однако через несколько лет у подавляющего большинства больных БП, принимающих леводопу, развиваются колебания эффекта (моторные флуктуации) и избыточные движения (дискинезии). С каждым годом приема леводопы распространенность моторных флуктуаций увеличивается в среднем на 10%.
Ранним проявлением флуктуаций служит постепенное уменьшение эффекта к концу действия разовой дозы леводопы с его укорочением ее до 3, а затем и до 2 часов, что приводит к усилению симптомов паркинсонизма в утренние часы или к моменту приема очередной дозы (развивается, так называемый, феномен «истощения» действия конца дозы). В результате в течение суток возникают колебания между относительно благополучным состоянием на фоне действия принятой дозы леводопы (период «включения») и состоянием относительной обездвиженности на фоне ослабления ее действия (период «выключения»).
По мере прогрессирования заболевания нарастает амплитуда колебаний между двумя состояниями, и переход от одного состояния к другому становится все более резким, при этом ухудшение двигательных функций в период «выключения» характеризуется рикошетным усилением симптомов, а не просто возвращением к их исходному уровню (феномен «включения-выключения»).
Со временем периоды «включения» и «выключения» теряют связь с приемом леводопы и становятся непредсказуемыми. Под влиянием случайных факторов (например, стресса) или спонтанно может наступить внезапное ухудшение состояния, несмотря на то, что недавно принятая доза только начала действовать, и столь же внезапное улучшение, иногда без дополнительного приема препарата.
Моторные флуктуации часто сопровождаются немоторными феноменами, связанными с колебаниями выраженности психических, сенсорных, вегетативных симптомов.
Главным фактором развития моторных флуктуаций является неуклонная дегенерация нигростриарных нейронов. Показано, что повторное назначение леводопы сопровождается укорочением длительности ее действия только в том случае, если погибло более 95% нигростриарных нейронов.
В результате уменьшения нигростриарных терминалей в стриатуме утрачивается их «буферная» функция — способность накапливать и плавно высвобождать дофамин, образуемый из экзогенной леводопы. В сохранившихся нейронах ускоряется кругооборот дофамина — клетки быстрее высвобождают дофамин, а не накапливают его в везикулах. Леводопа все в большей степени перерабатывается в дофамин в соседних глиальных и недофаминергических нейронах, в которых содержится ДОФА-декарбоксилаза, но отсутствует механизм, регулирующий продукцию дофамина, что приводит к массивному неконтролируемому высвобождению дофамина вскоре после приема очередной дозы. В результате концентрация дофамина в синапсе попадает в зависимость от колебаний уровня леводопы в крови.
Дофаминовые рецепторы таким образом подвергаются воздействию то высоких, то низких концентраций дофамина. Поэтому их стимуляция из тонической (в физиологических условиях) превращается в пульсирующую, что, в свою очередь, изменяет функциональное состояние постсинаптических структур — рецепторов аппарата и стриарных нейронов, что опосредовано изменениями на уровне генетического аппарата и продукции белков. Таким образом, есть данные о том, что в процесс возникновения моторных флуктуаций включаются как пре-, так и постсинаптические механизмы.
Вероятность развития моторных флуктуаций зависит не только от длительности и характера заболевания, но и от длительности лечения леводопой и ее суммарной дозы. Поэтому, чтобы отсрочить момент развития флуктуаций, часто пытаются отложить назначение препаратов леводопы. Тем не менее, у этой тактики есть ограничения: чем позднее по ходу развития заболевания назначается препарат леводопы, тем при прочих равных условиях быстрее развиваются флуктуации, поскольку процент сохранившихся нигростриарных терминалей в полосатом теле оказывается ниже. В связи с этим момент назначения леводопы правильнее определять исходя из основной задачи лечения — обеспечение индивидуально оптимального уровня двигательной активности пациента.
Важным фактором, влияющим на вероятность развития флуктуаций, является возраст начала заболевания. У молодых больных (при начале заболевания до 50 лет) флуктуации развиваются быстрее и чаще. Через 6 лет от начала заболевания они отмечаются практически у всех больных, принадлежащих к этой возрастной категории. Поэтому именно у этой категории больных назначение препаратов леводопы целесообразно отложить на более длительный срок, а при необходимости их назначения ограничиться минимальной эффективной дозой.
Помимо центральных фармакодинамических факторов на развитие флуктуаций могут оказывать влияние и периферические фармакокинетические факторы, которые играют решающую роль в замедленном наступлении эффекта (45—90 мин) или эпизодическом отсутствии эффекта принятой дозы леводопы. Их причиной может быть замедление опорожнение желудка вследствие нарушения вегетативной регуляции или стимуляции дофаминовых рецепторов в желудке, приводящей к ослаблению его моторики. В результате уровень леводопы не достигает критического порога. Этому способствует и прием леводопы вместе с пищей, содержащей аминокислоты, конкурирующие с ней за переносчики.
Развитие флуктуаций связывают и со способностью леводопы оказывать токсическое воздействие на культуру дофаминергических нейронов, выявленное в эксперименте. При окислении леводопы или образовавшегося из нее дофамина продуцируются свободные радикалы, которые могут спровоцировать перекисное окисление липидов и нарушить функционирование дыхательной цепи митохондрий и тем самым ускорять дегенеративный процесс. Однако доказательств, что этот эффект имеет место in vivo, получить не удалось. Более того, в эксперименте показано, что длительное назначение препаратов леводопы может оказывать и трофическое действие.
Своеобразным вариантом флуктуаций являются застывания — внезапная кратковременная блокада осуществляемого движения, чаще всего локомоторного, которая бывает спровоцирована началом ходьбы, поворотом, проходом через узкое пространство, столкновением и может быть преодолена с помощью различных внутренних или внешних стимулов (например, внутренними командами, напеванием мелодии и т.д.). Застывания могут возникать как в периоде «выключения», но и независимо от фазы действия леводопы. Застывания при БП чаще возникают на поздней стадии, их раннее развитие обычно указывает на иной диагноз (например, прогрессирующий надъядерный паралич).
Изменение реакции на леводопу проявляется и в снижении порога развития дискинезий. Через 5—7 лет лечения леводопой дискинезии выявляются у 50—80% больных, хотя тяжелые инвалидизирующие дискинезии встречаются реже. Дискинезии могут возникать в различные фазы действия леводопы: в период «выключения» (чаще в виде болезненной дистонии), на пике дозы (чаще в виде хореиформного гиперкинеза) или в начале и конце действия разовой дозы (двухфазные дискинезии — в виде баллистических или стереотипных движений ногами).
Гипотеза, связывающая развитие флуктуаций с пульсовой стимуляцией дофаминовых рецепторов, обусловленной коротким периодом полужизни препаратов леводопы, послужила основой для разработки препаратов леводопы с медленным (контролируемым) высвобождением, при применении которых колебания леводопы в плазме уменьшаются. Если обычные (стандартные) препараты леводопы растворяются в желудочно-кишечном тракте в течение 30 мин, то препарат с замедленным высвобождением — в течение 3 ч. В результате удлиняется период, течение которого в крови поддерживается терапевтическая концентрация леводопы, а в мозге — эффективная концентрация дофамина, что позволяет уменьшить выраженность феномена «истощения» действия конца дозы. Однако для препаратов с замедленным высвобождением характерна более низкая биодоступность леводопы, поэтому при переходе со стандартного препарата на препарат с замедленным высвобождением суточную дозу леводопы иногда приходится увеличивать на 20—30%, особенно на поздней стадии заболевания. Из-за замедленного наступления или отсутствия эффекта утренней дозы препарата с замедленным высвобождением у больных с поздней стадией заболевания может потребоваться дополнительный утренний прием стандартного препарата, содержащего леводопу. Предполагают, что раннее назначение препаратов с замедленным высвобождением леводопы может замедлять развитие флуктуаций за счет более длительной стимуляции дофаминовых рецепторов, однако это мнение не удалось пока подтвердить в контролируемых испытаниях. Тем не менее, препараты с замедленным высвобождением можно применять как на ранней, так и на поздней стадии заболевания.
При замедленном наступлении эффекта леводопы применяют также быстродействующую лекарственную форму леводопы, предполагающую растворение в жидкости непосредственно перед употреблением внутрь. Подобная форма позволяет быстро корригировать усиление симптомов паркинсонизма в ночные и ранние утренние часы (ночная акинезия, ранняя утренняя акинезия), связанное с истощением эффекта принятой накануне вечером дозы леводопы и нередко сопровождающееся затруднением глотания.
Агонисты дофаминергических рецепторов.
Агонисты дофаминергических рецепторов (АДР) способны непосредственно стимулировать дофаминовые рецепторы на стриарных нейронах в обход дегенерирующих нигростриарных клеток, имитируя действие эндогенного медиатора.
Первоначально АДР использовались как дополнение к леводопе на поздней стадии заболевания. Но в настоящее время АДР чаще используют в качестве монотерапии на ранней стадии БП, чтобы отсрочить назначение леводопы. Современные препараты АДР, назначаемые на ранней стадии БП, способны оказывать терапевтический эффект, сопоставимый с действием леводопы и тем самым позволяют отсрочить ее назначение на несколько лет. Исследования показывают, что монотерапия АДР практически не вызывает дискинезий и позволяет отсрочить развитие флуктуаций, но обычно ценой более низкой эффективности и более частых побочных эффектов (тошноты, отека голеней, повышенной сонливости, зрительных галлюцинаций).
Способность отодвигать момент развития флуктуаций может быть связана с тем, что, обладая длительным действием, агонисты дофаминергических рецепторов обеспечивают длительную квазифизиологическую стимуляцию дофаминовых рецепторов в полосатом теле.
С увеличением длительности лечения эффективность агонистов дофаминергических рецепторов снижается, что требует дополнительного назначения препараты леводопы. Через 2 года от момента начала лечения не менее чем двум третям больным приходится дополнительно назначать препараты леводопы, через 5 лет на монотерапии агонистов дофаминергических рецепторов обычно остаются не более 10—15% больных. При добавлении леводопы к агонистам дофаминергических рецепторов риск осложнений (таких, как дискинезии и флуктуации) повышается.
У больных с поздней стадией БП назначение агонистов дофаминергических рецепторов позволяет ослабить феномен «истощения» конца действия дозы, уменьшить длительность периода «выключения» и выраженность связанных с ним дискинезий, снизить дозу препарата леводопы. В тех случаях, когда добавление агонистов дофаминергических рецепторов позволяет снизить дозу препарата леводопы, это приводит и к ослаблению дискинезий «пика дозы», но этот эффект менее стойкий и не подтвержден в контролируемых исследованиях.
Агонисты дофаминергических рецепторов подразделяют на два класса — эрголиновые (бромокриптин, перголида мезилат, каберголин) и неэрголиновые (апоморфин, прамипексол, пирибедил). Достоинством неэрголиновых агонистов дофаминергических рецепторов является узкий спектр побочных эффектов, не включающий вазоспазм, эритромелалгию, плевропульмональный и забрюшинный фиброз.
Сравнительных исследований различных агонистов дофаминергических рецепторов проведено недостаточно, что затрудняет выбор препаратов. В целом, можно сделать вывод, что в эквивалентных дозах различные агонисты дофаминергических рецепторов оказывают сопоставимый эффект, но отличаются различной переносимостью. Например, из-за побочных эффектов дозу бромокриптина часто не удается повысить до эффективной. Поэтому в большинстве проведенных сравнительных исследований бромокриптин оказывается менее эффективен, чем другие агонисты дофаминергических рецепторов, особенно нового поколения (такие, как прамипексол).
Экспериментальные данные показывают, что агонисты дофаминергических рецепторов могут оказывать нейропротекторный эффект. О наличии этого эффекта косвенно свидетельствуют данные функциональной нейровизуализации, выявляющей более низкую скорость утраты маркеров дофаминергических окончаний в стриатуме на фоне приема агонистов дофаминергических рецепторов, чем на фоне приема леводопы, что, возможно, отражает замедление дегенеративного процесса. Тем не менее, на данный момент нейропротекторный эффект агонистов дофаминергических рецепторов не может считаться доказанным — до тех пор, пока он не будет подтвержден в контролируемых клинических испытаниях.
Ингибиторы катехол-О-метилтрансферазы.
Ингибиторы катехол-О-метилтрансферазы (энтакапон, толкапон) блокируют периферический метаболизм леводопы, удлиняют период ее полужизни в крови на 30—50% и тем самым увеличивают количество леводопы, поступающей в мозг. Соответственно удлиняется время, в течение которого уровень леводопы остается в терапевтическом диапазоне, и продолжительность эффекта каждой принятой дозы леводопы.
Основное показание к назначению ингибитора катехол-О-метилтрансферазы — наличие феномена «истощения» действия конца дозы. Наиболее частый побочный эффект — усиление дискинезий, при этом ингибиторы катехол-О-метилтрансферазы не столько увеличивают их интенсивность, сколько удлиняют их. Возможно также появление тошноты, ортостатической гипотензии, зрительных галлюцинаций, нарушения сна, изменение окраски мочи, диареи. При приеме толкапона отмечены случаи тяжелого лекарственного гепатита с летальным исходом, поэтому при его назначении необходим регулярный контроль уровня печеночных ферментов. При приеме энтакапона повышения активности ферментов печени не отмечено, однако его доза должна быть уменьшена при печеночной недостаточности, при которой биодоступность препарата повышается.
В последние годы предпринимаются попытки раннего назначения ингибиторов катехол-О-метилтрансферазы в комбинации с препаратами леводопы — с тем, чтобы в максимальной степени сгладить колебания уровня леводопы в крови и отсрочить развитие флуктуаций. Хотя получены экспериментальные данные, свидетельствующие о возможной эффективности такого подхода, в контролируемых клинических испытаниях этот эффект не доказан.
Ингибиторы моноаминоксидазы В.
Моноаминооксидаза типа В способствует распаду дофамина на дегидроксифенилацетат и перекись водорода. Последняя может участвовать в окислительном повреждении дофаминергических нейронов. Блокада моноаминооксидаза типа В увеличивает концентрацию дофамина в синаптической щели и за счет торможения окислительного стресса может оказывать нейропротекторное действие, которое в клинических испытаниях доказать не удалось. В настоящее время в клинической практике применяется лишь один препарат, избирательно ингибирующий моноаминооксидаза типа В — селегилин. Помимо торможения моноаминооксидаза В, селегилин тормозит обратный захват дофамина из синаптической щели. В целом противопаркинсонический эффект селегилина невелик, хотя и способен отсрочить назначение леводопы на 8—10 месяцев. При монотерапии селегилин почти не оказывает побочного действия, хотя его метаболит метамфетамин иногда вызывает инсомнию (если препарат принимают позже 13 ч). Добавление селегилина к леводопе позволяет снизить ее дозу на 10—15%. При этом возможно ослабление феномена «истощения» действия конца дозы. В то же время селигилин способен провоцировать или усиливать, как периферические, так и центральные побочные эффекты леводопы (ортостатическую гипотензию, нарушение сердечного ритма, дискинезии, галлюцинации).
Препараты амантадина.
Препараты амантадина (амантадина хлорид, амантадина сульфат) казывают умеренное положительное действие на все проявления болезни и хорошо переносятся. Однако улушение при приеме амантадина нередко бывает кратковременным из-за развития толерантности. Механизм действия амантадина преимущественно связан с блокадой глутаматных NMDA-рецепторов, блокадой обратного захвата дофамина и норадреналина (амфетаминоподобным действием), мягким холинолитическим действием. В связи с малой эффективностью и недоказанностью нейропротекторного эффекта на ранней стадии амантадин в последние годы используют реже. Однако сравнительно недавно оказалось, что препарат эффективно подавляет дискинезии, вызванные леводопой, на поздней стадии БП, хотя и этот эффект в среднем сохраняется около 6 месяцев. Как и приеме холинолитиков, при применении амантадина возможны существенные центральные побочные эффекты в виде спутанности сознания, беспокойства, галлюцинаций, сухости во рту. У части больных развиваются отеки лодыжек и livedo reticularis (ретикулярная асфиксия — пурпурный сетчатый сосудистый рисунок на поверхности кожи).
Установлено, что улучшение при приеме амантадина имеет место у двух третей больных с ранней стадией. На поздней стадии добавление амантадина к леводопе оказывает дополнительное положительное действие.
Холинолитические препараты.
Холинолитики существенно менее эффективны, чем леводопа, и их применение оправдано главным образом при наличии тремора покоя. Применение холинолитиков ограничивают их побочные эффекта. Они вызывают мидриаз (и поэтому противопоказаны при закрытоугольной глаукоме), сухость во рту, провоцируют задержку мочи (особенно у мужчин с гиперплазией предстательной железы). Но наиболее серьезные побочные действия — усиление когнитивных нарушений и способность вызывать состояние спутанности и зрительные галлюцинации. Эти осложнения чаще возникают у лиц пожилого возраста.
Лечение вегетативных нарушений.
При клинически значимой ортостатической гипотензии лечение включает оптимизацию противопаркинсонической терапии со снижением избыточной дозы дофаминергических средств, ношение эластичных чулок, увеличение потребления поваренной соли (до 2 г в день) и жидкости (до 2 л в день) в отсутствие сердечной недостаточности; больным рекомендуют избегать резких изменений позы, спать на кровати с изголовьем, приподнятым на 15—20 см. При неэффективности этих мер назначают флудрокортизон (0,1—0,4 мг/сут) (противопоказан при сердечной, почечной и печеночной недостаточности) и (или) агонист альфа1-адренорецепторов мидодрин (15—30 мг/сут в 3—4 приема). При неэффективности этих средств возможно применение индометацина, кофеина, дигироэрготамина, десмопрессина (на ночь).
При клинически значимом нейрогенном нарушении мочеиспускания по типу гиперрефлексии детрузора по согласованию с урологом применяют трициклические антидепрессанты (мелипрамин, 10—50 мг/сут) или антихолинергические средства (оксибутинин, 5—30 мг/сут, или толтеродин, 2—4 мг/сут) в виде стандартных препаратов или препаратов длительного действия. Лечение проводится под контролем объема остаточной мочи, который не должен превышать 100 мл. При диссинергии детрузора и сфинктера или при наличии сопутствующей гиперплазии предстательной железы после урологического обследования у мужчин назначают антагонисты альфа-адренорецепторов (альфузозин, 5—7,5 мг/сут, доксазозин, 1—16 мг/сут, празозин, 1—10 мг/сут, тамсулозин, 0,4—0,8 мг/сут, или теразозин, 1—10 мг/сут). При выраженной никтурии возможно применение десмопрессина (под контролем уровня натрия в крови).
При ослаблении моторики желудочно-кишечного тракта рекомендуются модификация диеты с увеличением потребления пищевых волокон, отмена антихолинергических средств, назначение домперидона или цизаприда, эпизодическое применение слабительных.
Лечение когнитивных нарушений.
При прогрессировании когнитивного дефекта необходима оптимизация противопаркинсонической терапии, снижение дозы или постепенная отмена препаратов, способных оказывать отрицательное действие на познавательные функции. Эффективность ни одного из препаратов, усиливающих когнитивные функции, у больных болезнью Паркинсона не доказана в контролируемых клинических испытаниях. Тем не менее, в некоторых открытых исследованиях показан благоприятный эффект ингибиторов холинэстеразы (ривастигмина, донепезила, галантамина). На практике для лечения когнитивных нарушений применяют также мемантин, ипидакрин, холина альфосцерат, пирацетам, однако доказательств их эффективности при БП нет.
Лечение аффективных нарушений.
При наличии депрессии оптимизация противопаркинсонической терапии с назначением противопаркинсонических препаратов, обладающих антидепрессивным действием, прежде всего агонистов дофаминовых рецепторов (таких, как пирибедил или прамипексол) наряду с психотерапевтическим воздействием позволяет иногда добиться необходимого эффекта. Однако при выраженной депрессии становится необходимым назначение антидепрессантов. При БП эффективность ни одного антидепрессанта к настоящему времени не доказана, что позволяет использовать широкий спектр антидепрессантов, в том числе трициклические антидепрессанты, селективные ингибиторы обратного захвата серотонина, ингибиторы норадреналина, моноаминооксидаза типа А.
Лечение психотических нарушений.
Зрительные галлюцинации в большинстве случаев возникают на фоне сохранной ориентации и критики (так называемый «доброкачественный галлюциноз») и требуют планомерной коррекции схемы лечения. В первую очередь снижают дозу или отменяют недавно назначенное или наименее полезное средство, часто в следующем порядке — холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов. Даже если возникновение психотического расстройства связано с добавлением нового препарата, для устранения этого осложнения может потребоваться отмена другого средства. Например, если психотическое расстройство возникло при присоединении к комбинации леводопы и холинолитика агониста дофаминовых рецепторов, то постепенная отмена холинолитика может привести к нормализации психического статуса больного. Важно лишь своевременно выявлять «доброкачественный галлюциноз», поскольку многие больные в силу ряда причин не склонны сразу сообщать врачам о возникших у них необычных симптомах. В подобных случаях важно обращать внимание на предвестники психотических нарушений, в роли которых могут выступать: ночные кошмары, акатизия, психомоторное возбуждение, расторможенность, эпизоды пространственно-временной дезориентации, «пандинг» (бессмысленное перебирание предметов), миоклония, эйфория. Если коррекция противопаркинсонической терапии не будет своевременно произведена, то может галлюцинации могут приобрести угрожающий характер, критика снижается, присоединяются бредовые нарушения. В конечном итоге может развиться делирий, требующий госпитализации больного и тщательного поиска иных (помимо лекарственных) причин развития психотического эпизода.
Лечение нарушений сна и бодрствования.
У значительного числа больных с БП нарушается сон, что часто требует коррекции схемы противопаркинсонической терапии. Иногда затруднение засыпания вызвано препаратами леводопы, агониста дофаминовых рецепторов или амантадина (обычно это наблюдается лишь в начале лечения) — в этом случает временно снизить или отменить вечернюю дозу препарата, оставив суточную дозу неизменной. Но значительно чаще нарушения сна и, прежде всего ночные пробуждения вызваны усилением симптомов паркинсонизма в ночное время (ночной акинезией), из-за чего, например, больным трудно повернуться в постели. В этом случае, наоборот, следует увеличить вечернюю дозу леводопы, или, лучше, заменить стандартный препарат леводопы средством пролонгированного действия либо назначить агонист дофаминовых рецепторов непосредственно перед сном. Удлинить действие леводопы можно также с помощью антагониста катехол-О-метилтрансферазы или селегилина. Если действие дофаминергических средств не удается «растянуть» на всю ночь, то больному рекомендуется дополнительно принять при пробуждении стандартный или быстродействующий препарат леводопы. В то же время, если расстройство сна обусловлено ночной акатизией, которая обычно провоцируется избыточным приемом леводопы, то необходимо уменьшить вечернюю дозу леводопы, а если эта мера оказывается недостаточной, то назначить на ночь клоназепам или небольшую дозу клозапина (6,25—12,5 мг), который может к тому же уменьшить ночной тремор, иногда являющийся причиной ночных пробуждений.
Если коррекция противопаркинсонической терапии не устранило инсомнию, то показано дополнительное назначение антидепрессантов с седативным действием (например, тразодона, амитриптилина, доксепина и др.). Снотворные бензодиазепинового ряда можно назначать лишь на очень короткий срок или эпизодически — не только из-за угрозы лекарственной зависимости или привыкания, но и из-за опасности усиления двигательных нарушений и возникновения спутанности сознания (особенно у больных с деменцией). При возникновении спутанности сознания в ночное время следует отменить назначенные ранее седативные препараты, бензодиазепины, особенно длительного действия (например, диазепам, феназепам и др.) и перераспределить суточную дозу дофаминергических средств, уменьшив дозу, назначаемую на ночь. При недостаточной эффективности этой меры на ночь можно назначить хлорметиазол, 300—600 мг на ночь. Ночные кошмары, вызываемые дофаминергическими средствами, могут быть предвестниками психотических нарушений при БП и требуют снижения дозы леводопы, назначаемой в вечернее время и на ночь. Если сон нарушается из-за необходимости часто вставать в туалет, то могут помочь умеренные дозы оксибутинина, 2,5—5 мг на ночь, толтеродина, 2 мг на ночь или трициклических антидепрессантов (амитриптилина, мелипрамина, 12,5—25 мг на ночь).
При повышенной дневной сонливости следует попытаться нормализовать ночной сон, выявить и провести коррекцию синдрома апноэ во сне, установить оптимальный для больного режим дневной активности, скорректировать ортостатическую гипотензию и гипотензию после приема пищи. Если гиперсомния связана с приемом избыточной дозы леводопы или АДР, следует рассмотреть возможность ее снижения. По возможности следует отменить другие препараты с седативным действием. Если указанные выше меры неэффективны или невозможны из-за угрозы усиления двигательных нарушений, то могут быть назначены селегилин или антидепрессанты со стимулирующим действием.
Ранняя стадия
Начало лечения.
Поскольку в настоящее время отсутствуют средства с доказанным нейропротекторным эффектом, лечение преимущественно имеет симптоматический характер, однако поскольку оно влияет на некоторые звенья патогенеза БП (например, дефицит дофамина в стриатуме), некоторые специалисты рассматривают его и как патогенетическое. Стратегическая цель лечения, которая во многом диктует его тактику, заключается в обеспечении оптимального уровня повседневной активности больного в течение максимально длительного периода. Врач, диагностировавший у своего пациента БП, должен решить, следует ли ему немедленно начинать терапию или отложить ее до развития более существенного двигательного дефекта; если начинать лечение, то каким препаратом.
Решение принимается с учетом не только чисто медицинских факторов (тяжесть заболевания и степени инвалидизации, психические статус, сопутствующие заболевания), но и социально-психологических факторов — социального статуса больного, особенностей его работы, его ожиданий.
Лечение принято начинать тогда, когда двигательный дефект существенно ограничит функциональные возможности больного: затруднит продолжение работы или ограничит бытовую независимость больного (рис. 21).
Леводопа — самое эффективное средство, дающее наиболее гарантированный эффект, однако ее терапевтический ресурс ограничен, прежде всего, в связи с почти неизбежным развитием моторных флуктуаций и дискинезий. Отсюда стремление по возможности отсрочить момент назначения леводопы, заменив ее другими средствами. В любом случае следует выбрать — что важнее для данного конкретного больного: более высокая двигательная активность в ближайшей перспективе или снижение риска развития флуктуаций в долгосрочной перспективе. В идеале это решение следует принять вместе с больным. Отсюда важность разъяснения больному цели лечения и формирования у него адекватных ожиданий и рационального отношения к болезни.
Исключительно важное значение при определении начальной терапии имеют возраст больного и состояние психических функций. У молодых больных (до 50 лет) в силу особенностей течения заболевания и большей длительности предстоящей жизни вероятность развития флуктуации и дискинезии существенно выше, поэтому лечение леводопой надо максимально отсрочить. Лечение в этой возрастной группе может быть начато с агонистов дофаминергических рецепторов, селегилина, амантадина или холлинолитика. Если максимальная терапевтическая доза агонистов дофаминергических рецепторов не обеспечивает достаточного эффекта, то к нему последовательно добавляют другие препараты, переходя на комбинированную терапию. И только если агонисты дофаминергических рецепторов и их комбинация с другими средствами не обеспечивает оптимальный уровень функционирования больного, к лечению добавляют малые дозы леводопы (в виде стандартного препарата или препарата с замедленным высвобождением).
При начале заболевания после 70 лет проблема флуктуаций и дискинезий стоит не столь остро — у пожилых флуктуации развиваются позднее и бывают слабее, к тому же у них короче период предстоящей жизни. Следует также учитывать, что пожилые хуже переносят комбинацию препаратов, а из-за когнитивных нарушений предрасположены к психическим осложнениям. Иногда выбор препарата ограничивают и сопутствующие заболевания. В этой возрастной категории лечение целесообразно начинать с леводопы (в виде стандартного препарата или препарата с замедленным высвобождением). Холинолитики, ухудшающие когнитивные функции и способные вызвать спутанность сознания, обычно не назначают, а агонисты дофаминергических рецепторов, амантадин или селегилин с осторожностью присоединяют в последующем (обычно лишь при развитии флуктуаций и дискинезий).
В возрасте 50—70 лет лечение начинают с агонистов дофаминергических рецепторов при малой или умеренной выраженности двигательного дефекта и в отсутствие выраженных когнитивных нарушений, предрасполагающих к развитию побочных эффектов. В остальных случаях лечение начинают с препаратов леводопы (стандартных или с замедленным высвобождением) либо с комбинации агонистов дофаминовых рецепторов и леводопы. Если лечение начато с монотерапии препаратом леводопы, то в том случае, когда сравнительно небольшие ее дозы (300—400 мг/сут) не приносят достаточного эффекта, во избежание дальнейшего повышения ее дозы к ней добавляют агонисты дофаминергических рецепторов.
Указанная возрастная граница относительна, и общий принцип заключается в том, что чем моложе больной, тем позже следует вводить препараты леводопы. Кроме того, решающее значение играет не столько хронологический, сколько биологический возраст больных. При существенном ослаблении когнитивных функций и деменции независимо от возраста препаратами выбора являются средства, содержащие леводопу, которая у этой категории больных вызывает меньше психических побочных явлений.
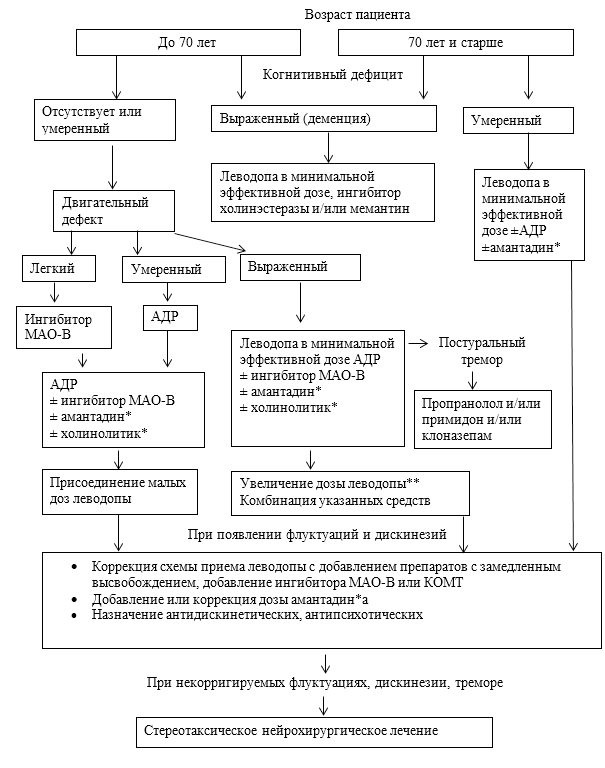
В период подбора терапии прием врача проводится не реже 1 раза в 4 недели. При осмотре следует обращать внимание на изменение выраженности основных симптомов паркинсонизма (гипокинезии, ригидности, тремора, постуральной неустойчивости) на фоне лечения и возможные побочные эффекты, требующие коррекции терапии (тошнота, ортостатическая гипотензия, сонливость или инсомния, дискинезии).
Поскольку дофаминергические препараты у больных с глаукомой могут повысить внутриглазное давление, перед их назначением у всех пациентов старше 40 лет следует измерить внутриглазное давление. В дальнейшем измерение внутриглазного давления проводят после подбора противопаркинсонической терапии (обычно на 2-м месяце лечения) либо при появлении жалоб на ухудшение зрения.
Измерение артериального давления на периферических артериях проводят с целью выявления ортостатической гипотензии.
Больным с запорами и другими проявлениями нарушения моторики желудочно-кишечного тракта показана диета с высоким содержанием пищевых волокон, при снижении массы тела показана диета с повышенным содержанием белковых продуктов, а также продуктов, богатых витаминами и микроэлементами; для подбора диеты назначается консультация врача-диетолога.
При ограничении подвижности и наличии скелетно-мышечных болей показано проведение лечебной физкультуры, включающей упражнение на растяжение мышц, поддержание гибкости и тренировку координации движений, физиотерапии, рефлексотерапии; в связи с этим назначаются консультации врача лечебной физкультуры, физиотерапевта, рефлексотерапевта.
Сообщение больному диагноза заболевания должно сопровождаться сообщением ему краткой информации о сути болезни, возможности ее лечения, прогнозе. При негативной эмоциональной реакции пациента на сообщение диагноза и наличии аффективных нарушений назначается консультация врача-психотерапевта для решения вопроса о целесообразности проведения аутогенной тренировки или других методов психотерапии (психологической адаптации, методов релаксации и медитации и т.д.).
Лечение имеет симптоматический характер. Фармакологические средства назначаются в том случае, если хотя бы одно из проявлений заболевания приводит к ограничению жизнедеятельности пациента.
Лечение начинается с монотерапии. Если препарат оказался неэффективным (нет регресса симптоматики в течение месяца после достижения максимальной дозы) или плохо переносится, его заменяют средством той же или другой фармакологической группы. При выборе препарата и его дозы следует стремиться не к полному устранению симптомов, а к существенному улучшению функций, позволяющему поддерживать бытовую и профессиональную активность.
При частичном эффекте (недостаточное улучшение функций) к принимаемому препарату последовательно добавляют лекарственные средства иной фармакологической группы.
Выбор препарата проводят с учетом возраста, выраженности двигательного дефекта, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента.
У лиц моложе 50 лет при умеренной выраженности двигательных нарушений назначают один из следующих препаратов (таб. 10):
— агонист дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин),
— ингибитор моноаминооксидазы типа В (селегелин),
— антихолинергические средства (тригексифенидил, бипериден),
— амантадин.
Предпочтительнее начинать с лечения с одного из агонистов дофаминовых рецепторов, которые обеспечивают поддержание уровня жизнедеятельности пациентов в течение длительного времени и позволяют отсрочить назначение препаратов, содержащих леводопу, и развитие осложнений долгосрочной терапии этими средствами на несколько лет.
Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности или поддержания повседневной активности и избежать побочного действия. Лечение пирибедилом начинают с дозы 50 мг 1 раз в день (днем или вечером — после основного приема пищи), в последующем суточную дозу увеличивают на 50 мг 1—2 раза в неделю до достижения необходимого эффекта, но не выше 250 мг в сутки (50 мг 5 раз в день). Лечение прамипексолом начинают с дозы 0,125 мг 3 раза в день (после еды), затем еженедельно дозу последовательно увеличивают до 0,25 мг 3 раза в день, 0,5 мг 3 раза в день, при недостаточном эффекте до 1 мг 3 раза в день и 1,5 мг 3 раза в день (максимальная доза 4,5 мг в сутки). Лечение бромокриптином начинают с дозы 2,5 мг 3 раза в день, в последующем дозу еженедельно последовательно увеличивают до 5 мг 3 раза в день, 7,5 мг 3 раза в день, 10 мг 3 раза в день, 10 мг 4 раза в день (максимальная доза 40 мг/сут).
При появлении тошноты в период титрования назначают домперидон. Тошнота появляется при приеме агонистов дофаминовых рецепторов, намного реже при приеме препаратов, содержащих леводопу. Домперидон назначают по 10 мг за 20 мин до приема очередной дозы агониста дофаминовых рецепторов.
При неэффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы.
Антихолинергические средства показаны при наличии выраженного тремора покоя и сохранности нейропсихологических функций. Хотя они у этой категории лиц они могут применяться в качестве средств первого выбора, более целесообразно их добавление к агонисту дофаминовых рецепторов, если последний не обеспечивает достаточного подавления тремора. При закрытоугольной глаукоме применение антихолинергических средств возможно лишь при крайней необходимости под регулярным контролем внутриглазного давления.
Лечение тригексифенидилом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Лечение бипериденом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Препарат предпочтительнее принимать после еды.
Лечение амантадином начинают с дозы 100 мг 2 раза в день, при недостаточном эффекте доза может быть увеличена до 100 мг 3 раза в день, в последующем до 100 мг 4—5 раз в день (максимальная доза 500 мг в сутки). Препарат предпочтительнее принимать после еды. Во избежание нарушения сна последний прием амантадина должен быть не позднее 18 часов.
Лечение селегилином начинают с дозы 5 мг утром, через 1 неделю дозу увеличивают до 5 мг 2 раза в день. Во избежание нарушения сна последний прием селегилина должен быть не позднее 13 часов. Препарат предпочтительнее принимать после еды.
Если указанные препараты в максимально переносимых дозах и их комбинация не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат, содержащий леводопу (стандартный препарат или препарат с замедленным высвобождением) в минимальной эффективной дозе.
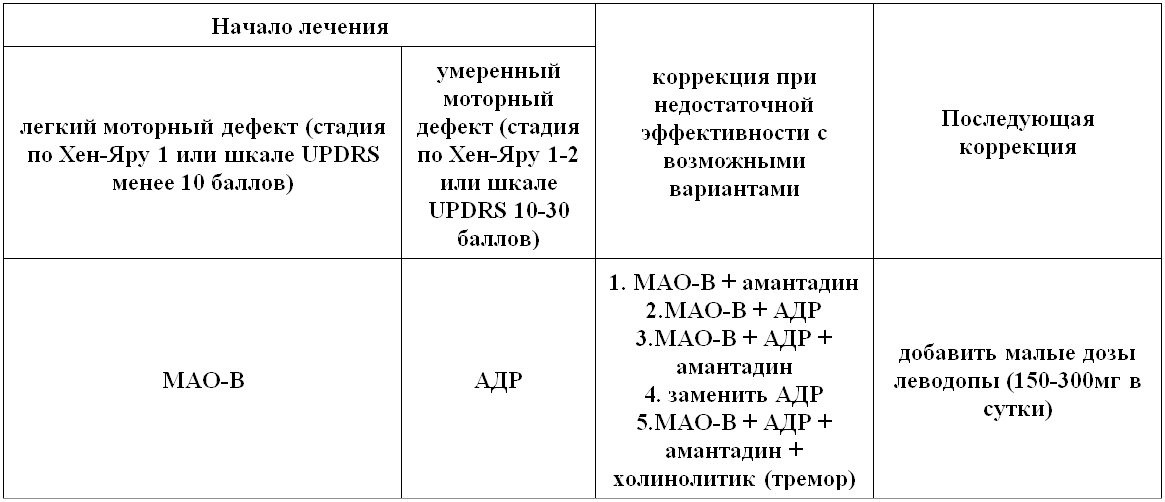
У лиц моложе 50 лет при наличии выраженного двигательного дефекта, ограничивающего их трудоспособность, лечение начинают с одной из двух комбинаций:
— комбинации агониста дофаминовых рецепторов (прамипексола, пирибедила, бромокриптина) и малых доз препарата, содержащего леводопу (200—400 мг леводопы в сутки);
— комбинации малых доз препарата, содержащего леводопу, с ингибитором катехол-О-метилтрансферазы энтакапоном или толкапоном.
Лечение агонистом дофаминовых рецепторов начинают по указанной выше схеме. Лечение препаратом, содержащим леводопу, начинают с дозы леводопы 50 мг 2 раза в день (в начале лечения препарат предпочтительнее принимать после еды). В последующем дозу увеличивают на чаще чем 1 раз в неделю последовательно до 50 мг 3 раза в день, 100 мг 3 раза в день, 100 мг 4 раза в день. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
Энтакапон назначают по 200 мг с каждым приемом средства, содержащего леводопу. Толкапон назначают по 100 мг 3 раза в день.
У лиц в возрасте 50—70 лет при умеренном двигательном дефекте и относительной сохранности нейропсихологических функций лечение начинают с одного из агонистов дофаминовых рецепторов (прамипексола, пирибедила, бромокриптина) (таб. 11).
Если максимальные переносимые дозы одного из этих препаратов не обеспечивают достаточного функционального улучшения, к нему последовательно добавляют по указанным выше схемам один из следующих препаратов:
— селегелин,
— амантадин,
— тригексифенидил или бипериден (при наличии тремора покоя). Больным после 65 лет тригексифенидил и другие антихолинергические средства не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов.
При недостаточной эффективности к комбинации из 2—3 указанных выше препаратов добавляют средство, содержащее леводопу, в минимальной эффективной дозе (200—400 мг леводопы в сутки). Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
У лиц в возрасте 50—70 лет при выраженном двигательном дефекте, ограничивающем трудоспособность и (или) возможность самообслуживания и необходимости получения быстрого эффекта, лечение начинают с препаратов, содержащих леводопу. Лечение препаратом, содержащим леводопу, начинают с дозы леводопы 50 мг 2 раза в день (в начале лечения препарат предпочтительнее принимать после еды). В последующем дозу увеличивают на чаще чем 1 раз в неделю последовательно до 50 мг 3 раза в день, 100 мг 3 раза в день, 100 мг 4 раза в день. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением.
Если небольшие дозы леводопы (200—400 мг леводопы в сутки) не обеспечивают необходимого улучшения, к ним последовательно добавляют по указанным выше схемам следующие препараты:
— агонист дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин),
— амантадин,
— ингибитор моноаминооксидазы типа В (селегилин),
— ингибитор катехол-О-метилтрансферазы (энтакапон или толкапон).

У пожилых лиц (старше 70 лет) лечение следует начинать со средств, содержащих леводопу (таб. 12). Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может снижать вероятность побочных действий на фоне пиковой концентрации препарата.
Особенности лечения больных с тремором. При выраженном дрожательном гиперкинезе, нарушающем функции конечностей, особенно если оно имеет постурально-кинетический компонент, к противопаркинсоническим средствам при отсутствии противопоказаний добавляют пропранолол. Лечение пропранололом начинают с дозы 10 мг 3 раза в день. В последующем дозу последовательно увеличивают не чаще чем 1 раз в неделю до 20 мг 3 раза в день, 40 мг 3 раза в день, 40 мг 4 раза в день (максимально до 320 мг в сутки в 3—4 приема).
При наличии противопоказаний к применению пропранолола (брадиаритмия, сахарный диабет, заболевания периферических сосудов), непереносимости или неэффективности препарата назначают примидон. Первоначально препарат назначают в дозе 31,25 мг на ночь, затем дозу последовательно увеличивают 1 раз в 7—10 дней до 62,5 мг на ночь, 125 мг на ночь, 250 мг на ночь (максимально до 750 мг в сутки в 2—4 приема или однократно на ночь).
Если пропранолол вызвал недостаточное улучшение, то к нему добавляют примидон в указанных дозах.

Клоназепам может быть добавлен к пропранололу или примидону при наличии выраженного кинетического компонента тремора. Клоназепам первоначально назначают в дозе 0,5 мг на ночь, затем 1 раз в 7—10 дней дозу последовательно увеличивают до 0,5 мг 2 раза в день, 1 мг 2 раза в день, 2 мг 2 раза в день, пока не будет достигнуто существенное ослабление дрожания.
При недостаточной эффективности пропранолола или примидона к ним добавляют антидепрессанты с седативным действием (амитриптилин, 12,5—50 мг на ночь, миртазапин, 7,5—15 мг на ночь).
В целом, дрожание хуже поддается лечению, чем другие симптомы паркинсонизма. Малые дозы леводопы могут даже усиливать тремор, возможно, за счет ослабления сдерживающего влияния акинезии и ригидности. Поэтому для лечения тремора часто необходимы более высокие дозы леводопы, связанным с риском побочных эффектов. Чтобы избежать преждевременной эскалации дозы леводопы, следует шире использовать агонисты дофаминергических рецепторов, которые у значительной части больных весьма эффективно подавляют тремор. Для усиления их эффекта можно применять холинолитики, пропранолол, амантадин, в наиболее резистентных случаях — клозапин. Если противопаркинсонические средства или их комбинация неэффективны — следует рассмотреть вопрос об оперативном лечении.
Особенности лечения больных с аффективными нарушениями. При наличии депрессии у больных без выраженных нарушений познавательных функций лечение следует начинать с одного из агонистов дофаминовых рецепторов (прамипексол, пирибедил), способных корригировать легкую депрессивную симптоматику, или их сочетания с малыми дозами леводопы.
При выраженной депрессивной симптоматике после консультации с психиатром показано назначение одного из следующих антидепрессантов:
— амитриптилин 25–150 мг на ночь,
— имипрамин 50–150 мг/сут,
— циталопрам, 20—40 мг/сут,
— флуоксетин, 20—40 мг/сут,
— сертралин, 50–100 мг/сут,
— пароксетин, 10—20 мг/сут,
— пирлиндол, 50—150 мг/сут,
— моклобемид, 150—300 мг/сут,
— миртазапин, 7,5—30 мг/сут,
— венлафаксин, 75—225 мг/сут.
Выбор антидепрессанта проводится с учетом индивидуальной чувствительности и риска побочных эффектов у данного больного. Следует избегать комбинации ингибитора обратного захвата серотонина с ингибитором моноаминооксидазы В селегилином в виду риска серотонинового синдрома. После получения лечебного эффекта продолжительность назначения антидепрессанта в эффективной дозе должна быть не менее 6 месяцев.
Лечение нарушений сна. При ночных побуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночной акинезией), прибегают к одной из следующих мер:
— увеличивают вечернюю дозу средства, содержащего леводопу,
— заменяют стандартный препарат леводопы средством пролонгированного действия,
— назначают агонист дофаминовых рецепторов (прамипексол, пирибедил, бромокриптин или каберголин) непосредственно перед сном.
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу, а если эта мера оказывается недостаточной, то назначают на ночь клоназепам.
При неэффективности указанных мер дополнительно назначают антидепрессант с седативным действием (тразодон, 75—150 мг, амитриптилин, 25—50 мг, или миртазапин, 15—30 мг).
Резистентность к лечению. Почти у всех больных с начальной стадией БП при применении тех или иных средств можно добиться ослабления симптомов. Тем не менее, у части пациентов улучшения добиться не удается. Самой частой причиной неэффективности терапии оказывается неправильный диагноз. Больные с мультисистемной атрофией, прогрессирующим надъядерным параличом, сосудистым паркинсонизмом, нормотензивной гидроцефалией и другими заболеваниями, вызывающими синдром паркинсонизма, в большинстве случаев резистентны к препаратам леводопы и другим противопаркинсоническим средствам. Причиной резистентности к терапии может быть также применение неэффективных у данного пациента противопаркинсонических препаратов или их необоснованно низких доз, прием препаратов, снижающих эффективность противопаркинсонической терапии (например, циннаризина или метоклопрамида). Ошибочное впечатление о неэффективности противопаркинсонической терапии может создавать депрессия, выявляемая почти у половины больных болезнью Паркинсона.
Ранняя, развернутая стадии
При стабильном состоянии больного прием врача проводится 2 раза в течение 6 месяцев.
При осмотре следует обращать внимание на изменение выраженности основных симптомов паркинсонизма (гипокинезии, ригидности, тремора, постуральной неустойчивости) на фоне лечения и возможные побочные эффекты, требующие коррекции терапии (тошнота, ортостатическая гипотензия, дневная сонливость или инсомния, дискинезии).
Поскольку дофаминергические препараты у больных с глаукомой могут повысить внутриглазное давление, перед их назначением у всех пациентов старше 40 лет следует измерить внутриглазное давление. Измерение внутриглазного давления проводят при появлении жалоб на ухудшение зрения.
Измерение артериального давления на периферических артериях проводят с целью выявления ортостатической гипотензии.
Больным с запорами и другими проявлениями нарушения моторики желудочно-кишечного тракта показана диета с высоким содержанием пищевых волокон, при снижении массы тела показана диета с повышенным содержанием белковых продуктов, а также, продуктов, богатых витаминами и микроэлементами; для подбора диеты назначается консультация врача-диетолога.
При ограничении подвижности и наличии скелетно-мышечных болей показано проведение лечебной физкультуры, включающей упражнение на растяжение мышц, поддержание гибкости и тренировку координации движений, физиотерапии, рефлексотерапии; в связи с этим назначаются консультации врача лечебной физкультуры, физиотерапевта, рефлексотерапевта.
При наличии аффективных нарушений назначается консультация врача-психотерапевта для решения вопроса о целесообразности проведения аутогенной тренировки или других методов психотерапии (психологической адаптации, методов релаксации и медитации и т.д.).
Проводится плановая коррекция противопаркинсонической терапии с целью поддержания адекватного уровня повседневной активности. При необходимости для усиления эффекта противопаркинсонической терапии проводятся следующие мероприятия:
1. Увеличение дозы принимаемого препарата, при необходимости до максимального рекомендуемого уровня (путем медленного титрования дозы):
— суточная доза препарата, содержащего леводопу, может быть увеличена на 50—100 мг не чаще, чем 1 раз в 2 недели, максимально до 800 мг/сут,
— суточная доза пирибедила может быть увеличена на 50 мг не чаще чем 1 раз в 2 недели, максимально до 250 мг/сут (в отсутствие приема препарата, содержащего леводопу) или 150 мг (при одновременном приеме препарата, содержащего леводопу),
— суточная доза бромокриптина может быть увеличена на 2,5—5 мг не чаще чем 1 раз в 2 недели, максимально до 40 мг/сут,
— суточная доза амантадина может быть увеличена на 100 мг не чаще чем 1 раз в 2 недели, максимально до 400 мг/сут,
— суточная доза селегилина может быть увеличена до 10 мг/сут,
— суточная доза тригексифенидила и биперидена может быть увеличена на 1—2 мг не чаще чем 1 раз в 2 недели, максимально до 10 мг/сут,
— доза толкапона может быть увеличена до 600 мг/сут.
2. Замена препарата, не оказавшего терапевтического эффекта в максимальной дозе или вызвавшего неприемлемое побочное действие даже в минимальной терапевтической дозе, препаратом из той же или другой фармакологической группы:
— замена препарата одной группы на препарат другой группы (например, холинолитика, амантадина или селегилина на агонист дофаминовых рецепторов) производится путем постепенной отмены принимавшегося ранее препарата с параллельным титрованием дозы вновь назначенного средства до получения эффекта (по схеме, указанной ниже). Во избежание рикошетного усиления симптоматики следует избегать внезапной отмены любого противопаркинсонического препарата, даже если он не оказывал видимого эффекта.
— замена принимаемого препарата на иной препарат этой же группы (например, одного агониста дофаминовых рецепторов на другой либо препарата леводопы с одним ингибитором ДОФА-декарбоксилазы (например, карбидопой) на препарат леводопы с другим ингибитором ДОФА-декарбоксилазы (например, бензеразидом) или наоборот).
3. Добавление к ранее назначенному средству, оказавшему частичный эффект, препарата другой группы с переходом от монотерапии к комбинированной терапии (например, к холинолитику или амантадину можно добавить агонист дофаминовых рецепторов, а к последнему — малые дозы леводопы). При комбинации препаратов их доза может быть снижена, что иногда обеспечивает хороший эффект при невысоком риске побочного действия. Доза вновь назначенного средства подбирается по следующим схемам.
Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности или поддержания повседневной активности и избежать побочного действия. Лечение пирибедилом начинают с дозы 50 мг 1 раз в день (днем или вечером — после основного приема пищи), в последующем суточную дозу увеличивают на 50 мг 1—2 раза в неделю до достижения необходимого эффекта, но не выше 250 мг в сутки (50 мг 5 раз в день). Лечение прамипексолом начинают с дозы 0,125 мг 3 раза в день (после еды), затем еженедельно дозу последовательно увеличивают до 0,25 мг 3 раза в день, 0,5 мг 3 раза в день, при недостаточном эффекте до 1 мг 3 раза в день и 1,5 мг 3 раза в день (максимальная доза 4,5 мг в сутки). Лечение бромокриптином начинают с дозы 2,5 мг 3 раза в день, в последующем дозу еженедельно последовательно увеличивают до 5 мг 3 раза в день, 7,5 мг 3 раза в день, 10 мг 3 раза в день, 10 мг 4 раза в день (максимальная доза 40 мг/сут).
При появлении тошноты в период титрования назначают домперидон. Тошнота появляется при приеме агонистов дофаминовых рецепторов, намного реже при приеме препаратов, содержащих леводопу. Домперидон назначают по 10 мг за 20 мин до приема очередной дозы агониста дофаминовых рецепторов.
При неэффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы.
Антихолинергические средства показаны при наличии выраженного тремора покоя и сохранности нейропсихологических функций. Хотя они у этой категории лиц они могут применяться в качестве средств первого выбора, более целесообразно их добавление к агонисту дофаминовых рецепторов, если последний не обеспечивает достаточного подавления тремора. При закрытоугольной глаукоме применение антихолинергических средств возможно лишь при крайней необходимости под регулярным контролем внутриглазного давления.
Лечение тригексифенидилом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Лечение бипериденом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Препарат предпочтительнее принимать после еды.
Лечение амантадином начинают с дозы 100 мг 2 раза в день, при недостаточном эффекте доза может быть увеличена до 100 мг 3 раза в день, в последующем до 100 мг 4—5 раз в день (максимальная доза 500 мг в сутки). Препарат предпочтительнее принимать после еды. Во избежание нарушения сна последний прием амантадина должен быть не позднее 18 часов.
Лечение селегилином начинают с дозы 5 мг утром, через 1 неделю дозу увеличивают до 5 мг 2 раза в день. Во избежание нарушения сна последний прием селегилина должен быть не позднее 13 часов. Препарат предпочтительнее принимать после еды.
Если указанные препараты в максимально переносимых дозах и их комбинация не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат, содержащий леводопу (стандартный препарат или препарат с замедленным высвобождением) в минимальной эффективной дозе.
Лечение препаратом, содержащим леводопу, начинают с дозы леводопы 50 мг 2 раза в день (в начале лечения препарат предпочтительнее принимать после еды). В последующем дозу увеличивают на чаще чем 1 раз в неделю последовательно до 50 мг 3 раза в день, 100 мг 3 раза в день, 100 мг 4 раза в день. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
Энтакапон назначают по 200 мг с каждым приемом средства, содержащего леводопу. Толкапон назначают по 100 мг 3 раза в день.
Если максимальные переносимые дозы одного из агонистов дофаминовых рецепторов (прамипексола, пирибедила, бромокриптина) не обеспечивают достаточного функционального улучшения, к нему последовательно добавляют по указанным выше схемам один из следующих препаратов:
— селегелин,
— амантадин,
— тригексифенидил или бипериден (при наличии тремора покоя). Больным после 65 лет тригексифенидил и другие антихолинергические средства не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов.
При недостаточной эффективности к комбинации из 2—3 указанных выше препаратов добавляют средство, содержащее леводопу, в минимальной эффективной дозе (200—400 мг леводопы в сутки). Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
Если небольшие дозы леводопы (200—400 мг леводопы в сутки) не обеспечивают необходимого улучшения, к ним последовательно добавляют по указанным выше схемам следующие препараты:
— агонист дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин),
— амантадин,
— ингибитор моноаминооксидазы типа В (селегилин),
— ингибитор катехол-О-метилтрансферазы (энтакапон или толкапон).
Особенности лечения больных с тремором. При выраженном дрожательном гиперкинезе, нарушающем функции конечностей, особенно если оно имеет постурально-кинетический компонент, к противопаркинсоническим средствам при отсутствии противопоказаний добавляют пропранолол в дозе от 60 до 320 мг/сут в 3—4 приема.
При наличии противопоказаний к применению пропранолола (брадиаритмия, сахарный диабет, заболевания периферических сосудов), непереносимости или неэффективности препарата назначают примидон в постепенно увеличивающейся дозе от 31,25 до 500 мг/сут в 2—4 приема или однократно на ночь.
Если пропранолол вызвал недостаточное улучшение, то к нему добавлют примидон в указанных дозах.
Клоназепам в дозе 0,5—2 мг однократно на ночь или в 2 приема может быть добавлен к пропранололу или примидону при наличии выраженного кинетического компонента тремора.
При недостаточной эффективности пропранолола или примидона к ним добавляют антидепрессанты с седативным действием (амитриптилин, 12,5—50 мг на ночь, миртазапин, 7,5—15 мг на ночь).
Особенности лечения больных с аффективными нарушениями. При наличии депрессии у больных без выраженных нарушений познавательных функций лечение следует начинать с одного из агонистов дофаминовых рецепторов (прамипексол, пирибедил), способных корригировать легкую депрессивную симптоматику.
При выраженной депрессивной симптоматике после консультации с психиатром показано назначение одного из следующих антидепрессантов:
— амитриптилин 25–150 мг на ночь,
— имипрамин 50–150 мг/сут,
— циталопрам, 20—40 мг/сут,
— флуоксетин, 20—40 мг/сут,
— сертралин, 50–100 мг/сут,
— пароксетин, 10—20 мг/сут,
— пирлиндол, 50—150 мг/сут,
— моклобемид, 150—300 мг/сут,
— миртазапин, 7,5—30 мг/сут,
— венлафаксин, 75—225 мг/сут.
Выбор антидепрессанта проводится с учетом риска побочных эффектов у данного больного. После получения эффекта прием антидепрессанта в эффективной дозе должен продолжаться не менее 6 месяцев. Следует избегать комбинации ингибитора обратного захвата серотонина с ингибитором моноаминооксидазы В селегилином в виду риска серотонинового синдрома.
Лечение нарушений сна. При ночных побуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночной акинезией), прибегают к одной из следующих мер:
— увеличивают вечернюю дозу средства, содержащего леводопу,
— заменяют стандартный препарат леводопы средством пролонгированного действия,
— назначают агонист дофаминовых рецепторов (прамипексол, пирибедил, бромокриптин или каберголин) непосредственно перед сном.
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу, а если эта мера оказывается недостаточной, то назначают на ночь клоназепам. При неэффективности указанных мер дополнительно назначают антидепрессант с седативным действием (тразодон, 75—150 мг, амитриптилин, 25—50 мг, или миртазапин, 15—30 мг).
Лечение ортостатической гипотензии. При ортостатической гипотензии, вызванной средствами, содержащими леводопу, и агонистами дофаминовых рецепторов, следует рассмотреть вопрос о возможности снижения дозы. При комбинированном лечении этими препаратами в первую очередь снижают дозу агонистов дофаминовых рецепторов. Если это невозможно из-за усиления двигательного дефекта, необходимы следующие меры:
— увеличение потребление соли (до 2 г/сут) и жидкости (до 2 л) в отсутствие признаков сердечной и почечной недостаточности,
— ношение эластичных чулок,
— поднятие изголовья кровати во время ночного сна на 15—20 см.
При неэффективности немедикаментозных мер дополнительно назначают флудрокортизон в дозе 0,1—0,4 мг/сут.
Развернутая поздняя стадия
В период подбора терапии прием невролога проводится не реже 1 раза в месяц с целью оценки лечебного эффекта терапии, своевременного выявления и коррекции побочных эффектов. Оценка лечебного эффекта предполагает:
— оценку изменения тяжести основных симптомов паркинсонизма после изменения схемы лечения,
— оценку длительности и равномерности действия средств, содержащих леводопу,
— оценку выраженности непроизвольных движений, степени их инвалидизирующего действия и времени их возникновения по отношению к фазам действия средств, содержащих леводопу,
— оценку наличия других побочных эффектов противопаркинсонических средств (зрительных галлюцинаций, ортостатической гипотензии, повышения внутриглазного давления).
При наличии запоров и других проявлений нарушения моторики желудочно-кишечного тракта показана диета с высоким содержанием пищевых волокон, при неравномерном эффекте средств, содержащих леводопу, в течение суток, требуется изменение диеты с ограничением приема продуктов, богатых пищевыми аминокислотами, в дневное время и приемом их в вечернее время; для подбора диеты назначается консультация врача-диетолога.
При ограничении подвижности и наличии скелетно-мышечных болей показано проведение лечебной физкультуры, включающей упражнение на растяжение мышц, поддержание гибкости и тренировку координации движений, массажа и физиотерапии, рефлексотерапии; в связи с этим назначаются консультации врача лечебной физкультуры, физиотерапевта, рефлексотерапевта.
При наличии аффективных нарушений назначается консультация врача-психотерапевта для решения вопроса о целесообразности проведения аутогенной тренировки или других методов психотерапии (психологической адаптации, методов релаксации и медитации и т.д.).
Если, несмотря на коррекцию схемы приема противопаркинсонических средств, сохраняются непроизвольные движения или нестабильность эффекта средств, содержащих леводопу, которые существенно ограничивают жизнедеятельность пациента (снижают трудоспособность или возможность самообслуживания), показана консультация нейрохирурга, специализирующегося в стереотаксической нейрохирургии, для решения вопроса о целесообразности нейрохирургического решения.
Уменьшение длительности действия средств, содержащих леводопу. При усилении симптомов паркинсонизма к концу действия очередной дозы средства, содержащего леводопу, прибегают к одной из следующих мер:
— увеличению кратности приема средства, содержащего леводопу, до 4—6 раз при сохранении неизменной суточной дозы или ее минимальном увеличении,
— частичной замене стандартного препарата, содержащего леводопу, на препарат, содержащий леводопу, с замедленным высвобождением,
— добавление одного из агонистов дофаминовых рецепторов (прамипексола, пирибедила или бромокриптина),
— добавление ингибитора моноаминооксидазы типа В селегилина,
— добавление ингибитора катехол-О-метилтрансферазы энтакапона или толкапона.
Если одна из этих мер оказалась неэффективной, следует испробовать другую либо их комбинацию.
Доза вновь назначенного средства подбирается по следующим схемам.
Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности или поддержания повседневной активности и избежать побочного действия. Лечение пирибедилом начинают с дозы 50 мг 1 раз в день (днем или вечером — после основного приема пищи), в последующем суточную дозу увеличивают на 50 мг 1—2 раза в неделю до достижения необходимого эффекта, но не выше 250 мг в сутки (50 мг 5 раз в день). Лечение прамипексолом начинают с дозы 0,125 мг 3 раза в день (после еды), затем еженедельно дозу последовательно увеличивают до 0,25 мг 3 раза в день, 0,5 мг 3 раза в день, при недостаточном эффекте до 1 мг 3 раза в день и 1,5 мг 3 раза в день (максимальная доза 4,5 мг в сутки). Лечение бромокриптином начинают с дозы 2,5 мг 3 раза в день, в последующем дозу еженедельно последовательно увеличивают до 5 мг 3 раза в день, 7,5 мг 3 раза в день, 10 мг 3 раза в день, 10 мг 4 раза в день (максимальная доза 40 мг/сут).
При появлении тошноты в период титрования назначают домперидон. Тошнота появляется при приеме агонистов дофаминовых рецепторов, намного реже при приеме препаратов, содержащих леводопу. Домперидон назначают по 10 мг за 20 мин до приема очередной дозы агониста дофаминовых рецепторов.
При неэффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы.
Антихолинергические средства показаны при наличии выраженного тремора покоя и сохранности нейропсихологических функций. Хотя они у этой категории лиц они могут применяться в качестве средств первого выбора, более целесообразно их добавление к агонисту дофаминовых рецепторов, если последний не обеспечивает достаточного подавления тремора. При закрытоугольной глаукоме применение антихолинергических средств возможно лишь при крайней необходимости под регулярным контролем внутриглазного давления.
Лечение тригексифенидилом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Лечение бипериденом начинают с дозы 1 мг 2 раза в день, в последующем дозу не чаще чем раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза 10 мг в сутки). Препарат предпочтительнее принимать после еды.
Лечение амантадином начинают с дозы 100 мг 2 раза в день, при недостаточном эффекте доза может быть увеличена до 100 мг 3 раза в день, в последующем до 100 мг 4—5 раз в день (максимальная доза 500 мг в сутки). Препарат предпочтительнее принимать после еды. Во избежание нарушения сна последний прием амантадина должен быть не позднее 18 часов.
Лечение селегилином начинают с дозы 5 мг утром, через 1 неделю дозу увеличивают до 5 мг 2 раза в день. Во избежание нарушения сна последний прием селегилина должен быть не позднее 13 часов. Препарат предпочтительнее принимать после еды.
Если указанные препараты в максимально переносимых дозах и их комбинация не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат, содержащий леводопу (стандартный препарат или препарат с замедленным высвобождением) в минимальной эффективной дозе.
Лечение препаратом, содержащим леводопу, начинают с дозы леводопы 50 мг 2 раза в день (в начале лечения препарат предпочтительнее принимать после еды). В последующем дозу увеличивают на чаще чем 1 раз в неделю последовательно до 50 мг 3 раза в день, 100 мг 3 раза в день, 100 мг 4 раза в день. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
Энтакапон назначают по 200 мг с каждым приемом средства, содержащего леводопу. Толкапон назначают по 100 мг 3 раза в день.
Если максимальные переносимые дозы одного из агонистов дофаминовых рецепторов (прамипексола, пирибедила, бромокриптина) не обеспечивают достаточного функционального улучшения, к нему последовательно добавляют по указанным выше схемам один из следующих препаратов:
— селегелин,
— амантадин,
— тригексифенидил или бипериден (при наличии тремора покоя). Больным после 65 лет тригексифенидил и другие антихолинергические средства не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов.
При недостаточной эффективности к комбинации из 2—3 указанных выше препаратов добавляют средство, содержащее леводопу, в минимальной эффективной дозе (200—400 мг леводопы в сутки). Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением. Преимущество препаратов с замедленным высвобождением заключается в более плавном изменении уровня леводопы в крови и отсутствии пикового увеличения ее концентрации, что может уменьшать вероятность развития моторных флуктуаций.
Если небольшие дозы леводопы (200—400 мг леводопы в сутки) не обеспечивают необходимого улучшения, к ним последовательно добавляют по указанным выше схемам следующие препараты:
— агонист дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин),
— амантадин,
— ингибитор моноаминооксидазы типа В (селегилин),
— ингибитор катехол-О-метилтрансферазы (энтакапон или толкапон).
Замедленное наступление или отсутствие эффекта разовой дозы средства, содержащего леводопу. Если отдельные дозы препарата леводопы, принятые в течение дня, оказываются неэффективными, рекомендуют:
— прием препарата, содержащего леводопу, на пустой желудок (за 30—45 мин до еды),
— прием препарата леводопы в растворенном виде,
— соблюдение низкобелковой диеты в течение дня,
— назначение препаратов, усиливающих моторику желудка: домперидона и (или) цизаприда.
Непредсказуемые колебания эффекта разовой дозы средств, содержащих леводопу, в течение суток (синдром «включения-выключения»). При появлении эпизодов внезапного усиления симптомов паркинсонизма на фоне действия очередной дозы леводопы следует предпринять следующее:
— оценить адекватность доз леводопы (излишне малые дозы не обеспечивают полноценного длительного эффекта),
— увеличить разовую дозу леводопы, увеличив интервал между приемами препарата до 4—5 часов,
— добавить один из агонистов дофаминовых рецрепторов (прамипексол, пирибедил или бромокриптин),
— принимать средство, содержащее леводопу, за 40—45 мин до еды, ограничить употребление белков в дневное время, назначить препараты, усиливающие моторику желудочно-кишечного тракта (домперидон, цизаприд),
— при затянувшемся выключении — принимают препарат леводопы в растворенном виде.

Насильственные движения на высоте действия разовой дозы средства, содержащего леводопу (дискинезия пика дозы). Если на высоте действия препарата леводопы появляются насильственные движения, ограничивающие жизнедеятельность пациента, нужно предпринять следующие действия:
— добавить один из агонистов дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин), снизив дозу леводопы и постепенно отменив антихолинергический препарат,
— снизить дозу или отменить селегилин,
— частично заменить стандартное средство, содержащее леводопу, на средство с замедленным высвобождением (при этом возможно увеличение длительности насильственных движений, что требует отмены препарата с замедленным высвобождением),
— добавить амантадин,
— добавить клоназепам,
— добавить клозапин (в наиболее тяжелых случаях).
Насильственные движения в начале и конце действия разовой дозы средства, содержащего леводопу (двухфазные дискинезии). При двухфазных дискинезиях нужно предпринять следующие меры:
— увеличить разовую дозу леводопы, уменьшив число приемов (очередная доза должна быть принята не ранее, чем будет завершен полный цикл дискинезий),
— добавить один из агонистов дофаминовых рецепторов (прамипексол, пирибедил или бромокриптин), уменьшив дозу леводопы,
— отменить средство, содержащее леводопу, с замедленным высвобождением.
Дистония, вызванная прекращением действия очередной дозы средства, содержащего леводопу. При выраженных болезненных дистониях, вызываемых прекращением действия очередной дозы средства, содержащего леводопу, необходимы следующие меры:
— добавление средства, содержащего леводопу, с замедленным высвобождением, или частичная замена стандартного средства средством с замедленным высвобождением,
— добавление одного из агонистов дофаминовых рецепторов (прамипексола, пирибедила или бромокриптина),
— прием средства, содержащего леводопу, в растворенном виде,
— дополнительное назначение антихолинергического средства (в отсутствие нарушения познавательных функций), баклофена, клоназепама, тизанидина, препарата лития, или инъекция ботулотоксина в мышцы, вовлеченные в гиперкинез.

Особенности лечения больных с тремором. При наличии выраженного дрожания, нарушающего функции конечностей к указанным средствам при отсутствии противопоказаний добавляется бета-блокатор пропранолол в дозе 60—320 мг/сут в 3—4 приема. При наличии противопоказаний к применению пропранолола (брадиаритмия, сахарный диабет, заболевания периферических сосудов) или его неэффективности у больных с постурально-кинетическим компонентом назначается примидон в постепенно увеличивающейся дозе от 31,25 до 500 мг/сут однократно на ночь или 2—4 приема.
Если пропранолол оказал частичный эффект, то возможна его комбинация с примидоном.
Клоназепам в дозе 0,5—2 мг/сут на ночь или в 2 приема может быть добавлен к пропранололу или примидону при наличии выраженного кинетического компонента тремора.
При недостаточной эффективности пропранолола или примидона к ним могут быть также добавлены антидепрессанты с седативным действием (амитриптилин, 12,5—50 мг на ночь, миртазапин, 7,5—15 мг на ночь).
Лечение ортостатической гипотензии. При ортостатической гипотензии, вызванной средствами, содержащими леводопу, и агонистами дофаминовых рецепторов следует рассмотреть вопрос о возможности снижения дозы. При комбинированном лечении этими препаратами в первую очередь снижают дозу агонистов дофаминовых рецепторов. Если это невозможно из-за усиления двигательного дефекта, необходимы следующие меры:
— увеличение потребление соли (до 2 г/сут) и жидкости (в отсутствие признаков сердечной и почечной недостаточности),
— ношение эластичных чулок,
— поднятие изголовья кровати во время ночного сна на 15—20 см.
При неэффективности немедикаментозных мер дополнительно назначают флудрокортизон в дозе 0,1—0,4 мг вечером, мидодрин, 15—50 мг/сут в 3—4 приема.
Лечение психотических нарушений. При зрительных галлюцинациях, возникших на фоне ясного сознания, сохранности ориентации и критики после консультации с психиатром проводится плановая коррекция противопаркинсонической терапии.
В первую очередь снижают дозу или отменяют недавно назначенное или наименее эффективное средство, часто в следующем порядке — холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов — ингибитор катехол-О-аминотрансферазы.
При сохранении галлюцинаций следует снизить дозу средства, содержащего леводопу, до минимального эффективного уровня, обеспечивающего необходимый уровень двигательной активности.
При неэффективности этой меры или невозможности снизить дозу средства, содержащего леводопу, из-за нарастания двигательного дефекта, назначается атипичный нейролептик клозапин в дозе от 6,25 до 50 мг на ночь. После регресса галлюциноза препарат может быть постепенно отменен в течение 1—2 недель.
При неэффективности или непереносимости клозапина могут быть назначены:
— кветиапин, 25—200 мг/сут,
— оланзапин, 2,5—15 мг/сут,
— рисперидон, 0,25—2 мг/сут,
— тиоридазин, 10—50 мг/сут,
— сульпирид, 50—400 мг/сут,
— галоперидол, 0,375—1,5 мг/сут.
При сочетании зрительных галлюцинаций с бредовыми нарушениями или при их возникновении на фоне спутанности сознании с развитием делирия, необходима консультация психиатра и госпитализация в психосоматическое отделение. Дальнейшее ведение пациента проводится в соответствие с другим протоколом.
Лечение аффективных и других психических нарушений. При наличии суточных колебаний аффективного состояния, связанных с колебаниями эффекта средств, содержащих леводопу, необходима коррекция схемы противопаркинсонической терапии по указанным выше алгоритмам. При легкой депрессии возможна оптимизация схемы противопаркинсонической терапии с назначением агонистов дофаминовых рецепторов (прамипексол, пирибедил).
При выраженной депрессивной симптоматике после консультации с психиатром показано назначение одного из следующих антидепрессантов:
— амитриптилин 25–150 мг на ночь,
— имипрамин 50–150 мг/сут,
— циталопрам, 20—40 мг/сут,
— флуоксетин, 20—40 мг/сут,
— сертралин, 50–100 мг/сут,
— пароксетин, 10—20 мг/сут,
— пирлиндол, 50—150 мг/сут,
— моклобемид, 150—300 мг/сут,
— миртазапин, 7,5—30 мг/сут,
— венлафаксин, 75—225 мг/сут.
Выбор антидепрессанта проводится с учетом риска побочных эффектов у данного больного. С учетом более низкого риска побочных эффектов со стороны сердечно-сосудистой системы, а также холинолитического действия у пожилых больных препаратами выбора являются селективные ингибиторы обратного захвата серотонина. Следует избегать комбинации селективного ингибитора обратного захвата серотонина с ингибитором моноаминоксидазы В селегилином ввиду риска серотонинового синдрома.
При синдроме навязчивых состояний лечение проводится антидепрессантами. Препаратами выбора являются кломипрамин и селективные ингибиторы обратного захвата серотонина сертралин, флуоксетин, циталопрам, пароксетин.
Лечение нарушений сна. При ночных пробуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночной акинезией), прибегают к одной из следующих мер:
— увеличивают вечернюю дозу средства, содержащего леводопу,
— заменяют стандартный препарат леводопы средством пролонгированного действия,
— назначают агонист дофаминовых рецепторов (прамипексол, пирибедил, бромокриптин или каберголин) непосредственно перед сном.
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу, а если эта мера оказывается недостаточной, то назначают на ночь клоназепам. При неэффективности указанных мер дополнительно назначают антидепрессант с седативным действием (тразодон, 75—150 мг, амитриптилин, 25—50 мг, или миртазапин, 15—30 мг).
Развернутая, поздняя, прогрессирующая стадии
Бесплатный фрагмент закончился.
Купите книгу, чтобы продолжить чтение.
